
题目列表(包括答案和解析)
1.人体内所必需的下列元素中,因摄入量不足而导致骨质疏松的是( )
A.K B.Ca C.Na D.Fe
26.(12分)CuSO4溶液和强碱反应得碱式硫酸铜,其化学组成为aCuSO4·bCu(OH)2(a、b
为正整数,且2<b<6,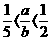 ),有的还含一定数目的结晶水,其组成随反应条件不同
),有的还含一定数目的结晶水,其组成随反应条件不同
而异。
(1)取一种不含结晶水的某碱式硫酸铜样品高温灼烧后只得CuO固体,另取等质量的该
样品,滴加稀盐酸至恰好完全反应。两次实验中消耗HCl与生成CuO的物质的量
之比为3:2,则该碱式硫酸铜的化学组成为__________________。
(2)某含结晶水的碱式硫酸铜aCuSO4·bCu(OH)2·cH20(c也是正整数),已知a+b+c=9。
取一定量样品高温灼烧至质量不再改变,将反应产生的气体通过盛有足量P205的U
型管,U型管增重1.26g。残留固体冷却后质量为5.60g。通过计算求该含结晶水
的碱式硫酸铜的化学组成。
25.(7分)用石墨电极电解500mLNaNO3和Cu(NO3)2的混合溶液。通电一段时间后,阴、
阳两极逸出的气体在标准状况下的体积分别为11.2L和8.4L,求原溶液中Cu2+的物质的
量浓度。
24.(11分)药用有机物A为一种无色液体。从A出发可发生如下一系列反应

试回答:
(1)化合物A、B的结构简式:A____________________;B___________________。
(2)用化学方程式表示反应③和④
③_________________________________________________________。
④_________________________________________________________。
(3)有机物A的同分异构体甚多,其中属于羧酸类化合物,且含有苯环结构的异构体有
4种,它们是____________、______________、______________、_____________。
23.(9分)CH3COOH是一种弱酸,而氯乙酸(CH2ClCOOH)的酸性强于CH3COOH,这是
因为-Cl是一种强吸引电子基团,能使-OH上的H 原子具有更大的活动性。有的基团
属于斥电子基团,能减弱-OH上H 原子的活动性,这种作用叫“诱导效应”。
根据以上规律判断:
(1)HCOOH 显酸性,而H2O 呈中性,这是由于HCOOH分子中存在__ __电子基
团,这种基团是___ ______。( )
(A)吸,羟基 (B) 吸,羧基 (C)斥,羧基 (D) 斥,羟基
(2)CH3COOH 的酸性弱于HCOOH,这是由于CH3COOH 分子中存在(斥)电子基团,
这种基团是(甲基)。 请判断:( )。 (填“对”或“错:)
(3)C6H5-(苯基)也属于吸电子基团,所以C6H5COOH(苯甲酸)酸性比乙酸的酸性
( )。(填 1---“强”或
2---“弱”)。 
22.(10分)现代生活中,人们越来越注意微量元素的摄入,碘元素对人体健康与发育有着
至关重要的作用。若缺少碘元素,则会造成幼儿痴呆、发育不良,易患地方性甲状腺肿。
为了预防碘缺乏病,我国卫生部规定每千克食盐中应含有40-50毫克的碘酸钾。
据此回答下列问题:
(1)食盐包装袋通常标有如下建议:菜未熟不宜加入碘盐。请简述其中所包含的化学原
理:_________________________________________________________________。_标有如下建议:菜未熟不宜加入碘盐。请简述其中所包含的化学原理。
(2)已知KIO3可用电解方法制得,原理是:以石墨为阳极,以不锈钢为阴极,在一定
电流强度和温度下电解KI溶液。总反应化学方程式为KI+3H2O KIO3十3H2↑
KIO3十3H2↑
则两极反应式分别为:阴极____________ _______,阳极__________ ______。
(3)为检验某食盐中是否含有碘酸钾。某同学取食盐样品428g溶解后,加入盐酸酸化
的淀粉碘化钾溶液,溶液呈蓝色。反应的离子方程式为_____________ ______,
氧化产物与还原产物的物质的量之比为________________ __。
(4)为进一步确证该样品是否为合格产品,该生再用0.030mol/L的硫代硫酸钠溶液滴
定,当用去18.00mL时蓝色刚好又褪去(I2+2S2O32--→2I-+S4O62-)由此可通过计算判
断该加碘食盐为____________ (填合格或不合格)食盐。
21.(10分)A、B、C、D、E均为常见的分子或离子,它们都具有10个电子,A是有五个
原子核的离子,它们之间的关系如下: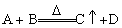 ,B+E=2D,D与酸性氧化物
,B+E=2D,D与酸性氧化物
和碱性氧化物均反应,则A的符号为________________,B的符号为________________,
E的电子式为_____ _________________。实验室制取C的化学方程式为
_______________________________________________ _________。
20.(10分)实验室有下列装置
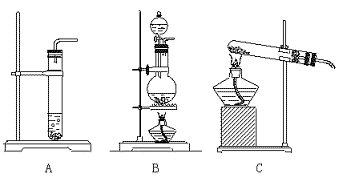
下列试剂:①一定浓度的氢氧化钠溶液 ②37%盐酸 ③40%硫酸 ④14%盐酸
⑤大理石 ⑥碳酸钾固体
按下列要求填空:
(1)要制取二氧化碳气体,应选用哪种装置__________________(填符号),选用哪些
试剂__________________(填代号),该装置检验气密性的方法_________
______________________________________________________________________,
有关的反应方程式____________________________________。
(2)制备碳酸钠的纯溶液,应选择的试剂为_____ ___(填代号),简述试验步骤。
19. (9分)实验室用如图所示方法制Fe(OH)2,但一般看不到白色沉淀,
(9分)实验室用如图所示方法制Fe(OH)2,但一般看不到白色沉淀,
而是灰绿色转为红褐色的沉淀,请回答:
(1)滴管下端插入液面的原因是_____________________________
______________________________________________。
(2)生成红褐色沉淀的化学方程式为_________________________。
(3)此反应中的02可能来自于______________________________
_____________________________________________________。
(4)现欲用同样的装置制得Fe(OH)2白色沉淀(至少能存在较长的时间),
设计一个改良的实验方案。(提示:如何能减少02对生成Fe(OH)2的氧化)
|
操 作 方 法 |
目 的 |
|
|
|
|
|
|
|
|
|
|
|
|
18.化学工作者把烷烃、烯烃、环烷烃、炔烃、……的通式转化成键数的通式,给研究有机
物分子中键能大小的规律带来了很大方便。设键数为I,则烷烃中碳原子数跟键数的关
系的通式为CnI3n+1,烯烃(视双键为两条单键)、环烷烃中碳原子数跟键数关系的通式为
CnI3n,则苯的同系物中碳原子数跟键数关系的通式为 ( )
A.CnI3n-1 B.CnI3n-2 C.CnI3n-3 D.CnI3n-4
第Ⅱ卷(非选择题 共78分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com