
题目列表(包括答案和解析)
21.(10分)人体的胃液是一种无色而呈酸性的液体,pH在0.9-1.5之间,胃液中含有大量的盐酸,其中的H+浓度比血液高几万倍。回答下列问题:
胃液中含有大量的盐酸的意义是 ;
(2)若胃液酸度增高会患胃酸过多症,下列物质不适于用作治疗胃酸过多症的药物的主要成分的是 (A.小苏打粉 B.氢氧化铝粉C. 氧化钙粉D.纯碳酸钙粉)
(3)胃镜检查发现胃少量出血,说明溃疡以深及 (胃壁、胃粘膜下层),胃溃疡患者胃酸过多可考虑选用(2)中的试剂 。
(4)三硅酸镁晶体(Mg2Si3O8·nH2O)是一种常见的用来治疗胃溃疡的药物,该药物不溶于水,但能中和胃酸,作用持久。写出该药物中和胃酸的化学方程式: 。
20.(10分)X、Y、Z、W四种元素,都位于周期表中的短周期,且原子序数X<Y<Z<W。X原子和Y原子的最外层电子数之和与Z原子最外层电子数相等,X原子半径是自然界元素中原子半径最小的,W原子和Y原子最外层电子数之和为Z原子最外层电子数的2倍,W原子最外层电子数为其电子层数的3倍,推断这四种元素的名称分别为:X______ Y______ Z______ W_______
由X、Y、Z、W四种元素形成的一种有机酸盐,其原子数之比为4∶1∶1∶2,该化合物的名称为___________,其结构简式为___________。
19.(13分)磷化氢(PH3)是一种无色剧毒的气体(沸点为-89.70C)。夏夜,坟场附近游荡着的蓝莹莹的“鬼火”,就是PH3的自燃现象。PH3可以由碘化磷(PH4I)与强碱反应来制取,其原理类似于实验室制取氨气。现用下图所示装置进行PH3的制取和性质实验。
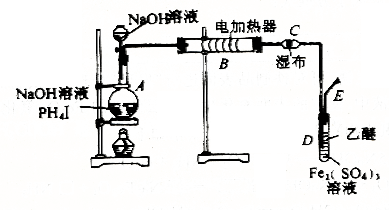
(1)实验室用PH4I和烧碱反应制取PH3的化学方程式为__________________;
(2)实验开始时,先从分液漏斗往盛有碘化磷的烧瓶(A)中加入适量的乙醚(乙醚为无色液体,沸点是34.5 ℃,微溶于水,与Fe2(SO4)3溶液不发生反应)。微热数分钟后,再从分液漏斗往烧瓶中加入一定量浓烧碱溶液,继续加热。在B处用电加热器控制硬质玻璃管温度在300℃左右。实验中可观察到:①在用湿布裹着的C管处有白色蜡状固体生成;②D试管中Fe2(SO4)3溶液由黄褐色变为浅绿色,同时也有白色蜡状固体生成;③E处点燃气体,火焰呈淡蓝色。
I.C管处白色蜡状固体是________,这一事实说明PH3受热________________。
II.D试管中发生反应的化学方程式为:__________________________,此反应说明PH3具有___________性。
III.E处导出的气体必须点燃的原因是___________________________________。
IV.实验开始时,先往烧瓶A中加入适量乙醚并加热,其目的是______________。
18.(6分)就氨的喷泉实验,回答下列问题:
(1)实验室欲快速制取大量氨气常用浓氨水加热,但当氨水浓度低于20%时,常向氨水中加入NaOH固体,此时仍能快速制取大量的氨气,其原因是:____________________;
(2)做完喷泉实验,在烧瓶内得到了氨水,为准确测定此氨水的物质的量浓度,可采用中和滴定的方法,中和滴定时,宜选用_________做指示剂。现有三种规格的锥形瓶:
A-50 mL 、 B-150 mL 、 C-500 mL, 若取20.00 mL氨水,应选用_________(填A、B、C)。现实验室有0.5mol/L、0.05mol/L和0.005mol/L的标准盐酸,中和滴定时宜选用________mol/L的标准盐酸。
17.胆固醇是人体必需的生物活性物质,分子式为C25H45O, 一种胆固醇酯是液晶材料,分子式为C32H49O2,生成这种胆固醇酯的酸是( )
A.C6H13COOH B.C6H5COOH
C.C7H15COOH D.C6H5 CH2 COOH
第II卷(非选择题 共78分)
16.在陶瓷和陶瓷器皿的釉质中含有极微量的Pb、Cd、Sb 等有毒的金属类,为防止中毒,不能长期盛放下列物质中的( )
A.酱油 B.食醋 C.蔗糖 D.食盐
15. 某短跑运动员经化验其体液中Ca2+ 含量太低,比赛时因神经肌肉的兴奋性升高而出现抽搐,这一事实说明Ca2+的生物功能之一是( )
A.构成生物细胞的组成之一 B.维持生物细胞的正常形态
C.维持生物细胞的正常生理功能 D.调整渗透压和酸碱平衡
14.具有解热镇痛及抗生素作用的“芬必得”主要成分的结构式是:
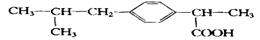
,它属于( )
A.芳香族化合物 B.苯甲酸的同系物
C.易溶于水的有机物 D.易升华的物质
13.人体中的血红蛋白中应含有Fe2+,如误食亚硝酸盐,则导致血红蛋白中的Fe2+转化为高铁血红蛋白而中毒,服用维生素C可解除亚硝酸盐中毒,下列叙述中正确的是( )
A.亚硝酸盐是还原剂 B.维生素C是氧化剂
C.维生素C将Fe3+转化为 Fe2+ D.亚硝酸盐被氧化
12.吸进人体中的氧气,有20%转化为氧化性极强的活性氧副产物,这些活性氧能加速人体衰老,被称为“生命杀手”,中国科学家尝试用含硒的化合物Na2SeO3清除体内的活性氧时,Na2SeO3的作用是( )
A.氧化剂
B.还原剂
C.既是氧化剂又是还原剂
D.既不是氧化剂又不是还原剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com