
题目列表(包括答案和解析)
19. (本小题共9分) 某同学用久置的(已部分氧化变质)绿矾配制纯净的FeSO4溶液,所选用的试剂有:蒸馏水、铁粉、稀硫酸。请回答下列问题:
(1)写出绿矾 FeSO4变质的化学反应方程式_______________________________。
(2)铁粉、稀硫酸的作用和有关的离子反应方程式分别是:铁粉__________________,稀硫酸____________________________________________
(3)配制过程中试剂的加入顺序为____________________________________________。
20.(本小题共14分) 某课外活动小组加热炭份(过量)和氧化铜的混合物,再用下图装置,对获得的铜粉(含炭)样品进行实验,请你帮助他们完成下列实验报告。
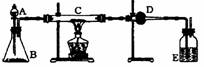 (一)实验目的:_________________________________。
(一)实验目的:_________________________________。
18.A、B、C、D、E分别是 Cu、Ag、Fe、Al、Mg五种金属中的一种。已知:(1)A、C均能与稀 H2SO4反应放出气体;(2)B与D的硝酸盐反应,置换出单质D;(3)C与强碱反应放出气体;(4)C、E在冷浓H2SO4中发生钝化反应,由此可以推断A、 B、 C、 D、E依次为 ( )
A. Fe、Cu、Al、Ag、Mg B.Al、Cu、Mg、Ag、Fe
C. Mg、Cu、Al、Ag、Fe D.Mg、Ag、Al、Cu、Fe
第II卷 (非选择题 满分78分)
17.下列各组溶液,无论将少量前者滴入后者,还是将少量后者滴入前者,生成物一定相同的是 ( )
A.AgNO3溶液和 NH3·H2O B.FeBr2溶液和氯水
C.NaOH溶液和AlC13溶液 D.Ca(HCO3)2溶液和澄清石灰水
16.以下描述的元素肯定是金属元素的是 ( )
A.原子最外层电子数≤3的元素
B.能与酸或碱反应放出氢气的元素
C.最外层电子数1~2个,次外层电子数8~18个的元素
D.核外电子层层数相同,内层均达饱和的几种离子中,离子半径最大的元素
15.工业上利用下述反应在真空中炼铷:2RbCl+ Mg==MgC12+ 2Rb。这一反应能进行的原因是 ( )
A.在高温下镁的金属活泼性比铷强
B.铷的沸点比镁低,以气体形式被抽去
C.铷的熔点比镁低,以液体形式被抽去
D.MgC12的稳定性比RbCl的强
14.二战期间丹麦科学家玻尔被迫离开德军占领的祖国。为了表明一定要返回祖国的决心,他把自己获得的金质诺贝尔奖章放在盛有王水的玻璃瓶中留了下来:Au+ HNO3+ 3HCl= AuCl3+ NO↑+ 2H2O;战后玻尔从溶液中提取金,又重新铸成了奖章,下列方法中,你认为不能从溶有黄金的王水中提取金的是 ( )
A.用铁置换 B.电解其水溶液
C.先蒸发水分后灼烧固体 D.过滤
|
13. 将锌、铁、铝、镁四种金属中的两种组成的混合物10g,与足量的盐酸反应产生的氢气在标准状况下为11.2 L,则混合物中一定含有的金属是 ( )
A. 锌 B. 铁 C. 铝 D. 镁
12.Fe(NO3)2溶液呈浅绿色,其中存在下列平衡:Fe2++2H2O = Fe(OH)2+2H+,往该溶液中逐滴加入盐酸,发生的变化是 ( )
A.平衡向正反应方向移动
B.平衡向逆反应方向移动
C.溶液颜色由浅绿色变为棕黄色
D.溶液由浅绿色变为灰绿色
11.最近,科学家冶炼出纯度高达99.999 %的铁,你估计它具有性质是 ( )
A.硬度比生铁小
B.在冷、浓H2SO4中可以钝化
C.在潮湿的空气中放置比生铁易生锈
D.当它与生铁的粉碎粒度相同时,与4mol/L盐酸反应速率比生铁大
10.混合下列各组物质使之充分反应,加热蒸干产物并在300℃灼烧至质量不变,最终残留固体为纯净物的是 ( )
A.向CuSO4溶液中加入适量铁粉
B.等物质的量浓度、等体积的(NH4)2SO4与 BaC12溶液
C.等物质的量的 NaHCO3与 Na2O2固体
D.在NaBr溶液中通入过量氯气
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com