
题目列表(包括答案和解析)
30.(6分)在一定条件下可实现下图所示物质之间的变化:请填写以下空

(1) 孔雀石的主要成分是CuCO3.Cu(OH)2(碱式碳酸铜),受热易分解。下图中的F是_____。
(2)写出明矾溶液与过量NaOH溶液反应的离子方程式___________________。
(3)图中所得G和D都为固体,混和后在高温下可发生反应,写出该反应的化学方程式: ______________________。
(4)每生成1摩D,同时生成____摩E。
29.(3分)一氧化氮是大气污染物之一。目前,有一种治理方法是在400℃左右、有催化剂存在的情况下,用氨把一氧化氮还原为氮气和水。请写出该反应的化学方程式______________________。
28.(9分)实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混和酸,加入反应器中。
②向室温下的混和酸中逐滴加入一定量的苯,充分振荡,混和均匀。
③在50-60℃下发生反应,直至反应结束。
④除去混和酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤。
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
填写下列空白:
(1)配制一定比例浓硫酸与浓硝酸混和酸时,操作注意事项是:______________________。
(2)步骤③中,为了使反应在50-60℃下进行,常用的方法是______________________。
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是______________________。
(4)步骤④中粗产品用5%NaOH溶液洗涤的目的是______________________。
(5)纯硝基苯是无色,密度比水_____(填“小”或“大”),具有_______气味的油状液体。
27.(6分)图(1)中瓶a内放入20毫升6摩/升盐酸,b是未充气的气球,里边放有4克碳酸钙粉未,将它套紧紧在瓶a口上,胶管c套在瓶的侧口,并用弹簧夹d夹紧(瓶口和侧口都不漏气)。将图(1)的装置在托盘天平上称量,质量为W1克。根据实验现象填写下列空白:
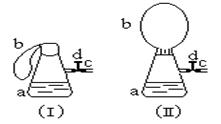
(1) 把气球b中的碳酸钙粉末小心地倒入瓶中,立即产生许多气泡,气球逐
渐胀大(图Ⅱ)。反应结束后,再次称量,质量为W2克。则W2和W1的关系是__________。
(2)取25毫升6摩/升NaOH溶液。先用滴管取少量NaOH溶液,滴管插入胶管c口(为便于操作,可以适当倾斜瓶a,注意防止漏气)。打开d,将溶液挤入瓶中,立即夹紧d。可以看到瓶内产生少量白色沉淀,轻轻摇动瓶a,沉淀随即消失。用同样方法再加入少量NaOH溶液,又产生白色沉淀,轻摇,沉淀又消失。使沉淀消失的反应的化学方程式是________________________。
(3)将全部NaOH溶液很快加入瓶中,加紧d,瓶内产生大量白色沉淀,不再溶解。此时瓶内温度__。(填“不变”、“降低”或“升高”)。
(4)继续轻摇瓶a,气球逐渐缩小,直至恢复反应前的下垂状。
写出这时发生的反应的化学方程式____________________________。
26.某温度下,在100克水中加入m克CuSO4或加入n克CuSO4.5H2O,均可使溶液恰好达到饱和,则 m与n的关系符合
A.m=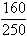 n B.m=
n B.m=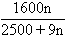 C.m=
C.m=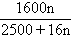 D.m=
D.m=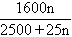
25.常温下,向20升真空容器内通入a摩硫化氢和b摩二氧化硫(a和b都是正整数,且a≤5,b≤5)。反应完全后,容器内气体可能达到的最大密度约是
A.24.5克/升 B.14.4克/升 C.8克/升 D.5.1克/升
24.在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6克X与Y完全反应后,生成4.4克R,则在此反应中Y和M的质量之比为 A.16:9 B.23:9 C.32:9 D.46:9
23.24毫升浓度为0.05摩/升的Na2SO3溶液,恰好与20毫升浓度为0.02摩/升的K2Cr2O7溶液完全反应,则元素Cr在被还原的产物中的化合价是 A.+6 B.+3 C.+2 D.0
22.下列各组溶液,不用其它试剂就可以将它们区别开的是
A.盐酸、氢氧化钾、硫酸钾、碳酸钾
B.硝酸钠、盐酸、氯化铵、氢氧化钾
B.氯化钡、氯化钙、硫酸钠、硝酸钾
D.氢氧化钾、碳酸钾、硫酸镁、硫酸氢钾
21.C1、C2、α1、α2,pH1,pH2分别表示2种一元弱酸的摩尔浓度、电离度和溶液的pH值如果已知 pH1<pH2,且α1>α2,则C1和C2的关系
A.C1>C2 B.C1=C2 C.C1<C2 D.无法确定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com