
题目列表(包括答案和解析)
24.在化合物X2Y和YZ2中,Y的质量百分比分别约为40%和50%,则在化合物X2YZ3中Y的质量百分比约为( )。 (A)20% (B)25% (C)30% (D)35%
23.120℃时,1体积某烃和4体积O2混和,完全燃烧后恢复到原来的温度和压强,体积不变,该烃分子式中所含的碳原子数不可能的是( )。 (A)1 (B)2 (C)3 (D)4
22.已知:t℃时,某物质不饱和溶液a克中含溶质m克。若该溶液蒸发b克水并恢复到t℃时,析出溶质m1克。若原溶液蒸发c克水并恢复到t℃时,则析出溶质m2克。用S表示该物质在t℃时的溶解度,下式中正确的是( )。
(A) (B)
(B)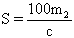 (C)
(C)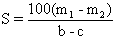 (D)
(D)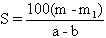
21.实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:今若制得Cl20.050摩,这时电池内消耗的H2SO4的物质的量至少是( )。 (A)0.025摩 (B)0.050摩 (C)0.10摩 (D)0.20摩
18.某溶液中有NH4+、Mg2+、Fe2+和Al3+四种离子,若向其中加入过量的氢氧化钠溶液
微热并搅拌, 再加入过量盐酸,溶液中大量减少的阳离子是( )。
(A)NH4+ (B)Mg2+ (C)Fe2+ (D)Al3+ 19.在同温同压下,下列各组热化学方程式中,Q2>Q1的是( )。 (A)2H2(气)+O2(气)=2H2O(气)+Q1 2H2(气)+O2(气)=2H2O(液)+Q2
(B)S(气)+O2(气)=SO2(气)+Q1 S(固)+O2(气)=SO2(气)+Q2
(C)C(固)+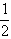 O2(气)=CO2(气)+Q1 C(固)+O2(气)=CO2(气)+Q2
O2(气)=CO2(气)+Q1 C(固)+O2(气)=CO2(气)+Q2
(D)H2(气)+Cl2(气)=2HCl(气)+Q1
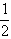 H2(气)+
H2(气)+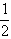 Cl2(气)=HCl(气)+Q2
20.下列说法正确的是(N0表示阿伏伽德罗常数的值)( )。
(A)标准状况下,以任意比例混和的甲烷和丙烷混和物22.4升,所含有的分子数为N0
(B)标准状况下,1升辛烷完全燃烧后,所生成气态产物的分子数为
Cl2(气)=HCl(气)+Q2
20.下列说法正确的是(N0表示阿伏伽德罗常数的值)( )。
(A)标准状况下,以任意比例混和的甲烷和丙烷混和物22.4升,所含有的分子数为N0
(B)标准状况下,1升辛烷完全燃烧后,所生成气态产物的分子数为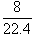 N0
(C)常温常压下,活泼金属从盐酸中置换出1摩H2,发生转移的电子数为2N0
(D)常温常压下,1摩氦气含有的核外电子数为4N0
三、选择题。(本小题包括6小题,每小题4分,共24分,每小题只有一个选项符合题意。)
N0
(C)常温常压下,活泼金属从盐酸中置换出1摩H2,发生转移的电子数为2N0
(D)常温常压下,1摩氦气含有的核外电子数为4N0
三、选择题。(本小题包括6小题,每小题4分,共24分,每小题只有一个选项符合题意。)
17.用10亳升的0.1摩/升BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的摩尔浓度之比是 (A)3:2:2 (B)1:2:3 (C)1:3:3 (D)3:1:1
16.描述CH3-CH=CH-C≡C-CF3分子结构的下列叙述中,正确的是( )。
(A)6个碳原子有可能都在一条直线上 (B)6个碳原子不可能都在一条直线上 (C)6个碳原子有可能都在同一平面上 (D)6个碳原子不可能都在同一平面上
15.某烃的一种同分异构体只能生成一种一氯代物,该烃的分子式可以是( )。 (A)C3H8 (B)C4H10 (C)C5H12 (D)C6H14
3.原子核外的M电子层和L电子层最多可容纳的电子数( )。 (A)大于 (B)小于 (C)等于 (D)不能肯定 4.钢和生铁中碳的百分含量( )。 (A)大于 (B)小于 (C)等于 (D)不能肯定 5.相同温度下的0.1摩/升和0.01摩升CH3COOH溶液中,CH3COOH的电离度( )。 (A)大于 (B)小于 (C)等于 (D)不能肯定 二、选择题。(本小题包括15小题,每小题3分,共45分,每小题有一个或两个选项符 合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给1分,选两个且都正确的给3分,但只要选错一个,该小题就为0分。) 6.科学家最近制造出第112号新元素,其原子的质量数为277,这是迄今已知元素中最重 的原子。关于该新元素的下列叙述正确的是( )。
(A)其原子核内中子数和质子数都是112 (B)其原子核内中子数为165,核外电子数为112 (C)其原子质量是12C原子质量的277倍 (D)其原子质量与12C原子质量之比为277:12 7.关于磷的下列叙述中,正确的是( )。 (A)红磷没有毒性而白磷剧毒 (B)白磷在空气中加热到260℃可转变为红磷 (C)白磷可用于制造安全火柴 (D)少量白磷应保存在水中 8.把三氯化铁溶液蒸干灼烧,最后得到的固体产物是( )。 (A)无水三氯化铁 (B)氢氧化铁 (C)氧化亚铁 (D)三氧化二铁 9.将1体积选项中的一种气体与10体积O2混和后,依次通过盛有足量浓NaOH溶液的洗 气瓶和盛有足量灼热铜屑的管子(假设反应都进行完全),最后得到的尾气是( ) (A)Cl2 (B)CO (C)CO2 (D)N2 10.关于化学键的下列叙述中,正确的是( )。 (A)离子化合物可能含共价键 (B)共价化合物可能含离子键 (C)离子化合物中只含离子键 (D)共价化合物中不含离子键 11.下列各组离子,在强碱性溶液中可以大量共存的是( )。 (A)K+、Na+、HSO3-、Cl- (B)Na+、Ba2+、AlO2-、NO3-
(C)NH4+、K+、Cl-、NO3- (D)K+、Na+、ClO-、S2- 12.下列离子方程式不正确的是( )。 (A)氨气通入稀硫酸溶液中NH3+H+=NH4+ (B)二氧化碳通入碳酸钠溶液中CO2+CO32-+H2O=2HCO3- (C)硫酸铝溶液跟偏铝酸钠溶液起反应Al3++3AlO2-+6H2O=4Al(OH)3↓
(D)氯气通入冷的氢氧化钠溶液中2Cl2+2OH-=3Cl-+ClO-+H2O
13.把氢氧化钙放入蒸馏水中,一定时间后达到如下平衡:Ca(OH)2(固)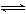 Ca2++2OH-
Ca2++2OH-
加入以下溶液可使Ca(OH)2减少的是( )。
(A)Na2S溶液 (B)AlCl3溶液 (C)NaOH溶液 (D)CaCl2溶液 14.X元素的阳离子和Y元素的阴离子具有与氩原子相同的电子层结构,下列叙述正确
的是( )。 (A)X的原子序数比Y的小 (B)X原子的最外层电子数比Y的大 (C)X的原子半径比Y的大 (D)X元素的最高正价比Y的小
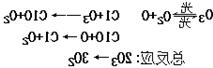 根据以下叙述,回答1-2小题。
1995年诺贝尔化学奖授予致力于研究臭氧层被破坏问题的三位环境化学家。大气中的臭氧层可滤除大量的紫外光,保护地球上的生物。氟利昂(如CCl2F2可在光的作用下分解,产生Cl原子,Cl原子会对臭氧层产生长久的破坏作用(臭氧的分子式为O3)。有关反应为:
根据以下叙述,回答1-2小题。
1995年诺贝尔化学奖授予致力于研究臭氧层被破坏问题的三位环境化学家。大气中的臭氧层可滤除大量的紫外光,保护地球上的生物。氟利昂(如CCl2F2可在光的作用下分解,产生Cl原子,Cl原子会对臭氧层产生长久的破坏作用(臭氧的分子式为O3)。有关反应为:
1.在上述臭氧变成氧气的反应过程中,Cl是( )。
(A)反应物 (B)生成物 (C)中间产物 (D)催化剂
2. O3和O2是( )。
(A)同分异构体 (B)同系物 (C)氧的同素异形体 (D)氧的同位素
请分别比较3-5三个小题中前后两个数值的相对大小。选择(A)、(B)、(C)、(D)表 示前者和后者的关系。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com