
题目列表(包括答案和解析)
37.(10分)现有一份CuO和Cu2O混合物,用H2还原法测定其中CuO的质量x(克).实验中可以测定如下数据:W-混合物的质量(克),WH2O-生成H2O的质量(克),WCu-生成Cu的质量(克),VH2-消耗的H2在标准状况下的体积(升) (已知摩尔质量:Cu-64克/摩尔、CuO-80克/摩尔、Cu2O-144克/摩尔、H2O-18克/摩尔) 组合共有几种,请将这些组合一一填入下表空格中. (1)为了计算x,至少需要测定上述四个数据中____个,这几个数据的饿组合共有_____种,
请 将这些组合一一填入下表格中。 说明:①选用W、WH2O、WCu、VH2表示,不必列出具体计算式. ②每个空格中填一种组合,有几种组合就填几种,不必填满.
(2)从上述组合中选出一个含W的求x的计算式: x=_______________________
的结构式是________________。 (2)化合物B是某种分子式为C9H12芳香烃一硝化后的唯一产物(硝基连在芳环上).化合物B的结 构式是__________________。 34. (3分)合成分子量在2000-50000范围内具有确定结构的有机化合物是一个新的研究领
域.1993年报道合成了两种烃A和B,其分子式分别为C1134H1146和C1398H1278.B分子比A相似,但
分子中多了一些结构为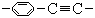 的结构单元。
B分子比A分子多了_________个这样的结构单元(填写数字).
的结构单元。
B分子比A分子多了_________个这样的结构单元(填写数字).
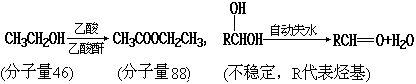
35.(11分)以乙烯为初始反应物可制得正丁醇(CH3CH2CH2CH2OH),已知两个醛分子在一定条件下可以自身加成.下式中反应的中间产物(Ⅲ)可看成是由(Ⅰ)中的碳氧双键打开,分别跟(Ⅱ)中的2-位碳原子和2-位氢原子相连而得.(Ⅲ)是一种3-羟基醛,此醛不稳定,受热即脱水而生成不饱和醛(烯醛):
 请运用已学过的知识和上述给出的信息写出由乙烯制正丁醇各步反应的化学方程式(不必写出
反应条件)____________________________________________________________.
七、(本题包括2小题,共17分)
36.(7分)称取0.200克某赤铁矿样品,矿样溶解后,使其中的铁全部转化成Fe2+(所得溶液中不含其他还原性物质).另称7.90克硫酸铈铵2(NH4)2SO2·Ce(SO4)2·2H2O(摩尔质量为632克/摩尔),溶解后稀释至250毫升.取该溶液30.0毫升恰好与上述Fe2+溶液完全反应.反应的离子方程式为:Ce4++Fe2+=Ce3++Fe3+.请计算该矿样中Fe2O3的质量百分含量)(Fe2O3摩尔质量为160克/摩尔).
请运用已学过的知识和上述给出的信息写出由乙烯制正丁醇各步反应的化学方程式(不必写出
反应条件)____________________________________________________________.
七、(本题包括2小题,共17分)
36.(7分)称取0.200克某赤铁矿样品,矿样溶解后,使其中的铁全部转化成Fe2+(所得溶液中不含其他还原性物质).另称7.90克硫酸铈铵2(NH4)2SO2·Ce(SO4)2·2H2O(摩尔质量为632克/摩尔),溶解后稀释至250毫升.取该溶液30.0毫升恰好与上述Fe2+溶液完全反应.反应的离子方程式为:Ce4++Fe2+=Ce3++Fe3+.请计算该矿样中Fe2O3的质量百分含量)(Fe2O3摩尔质量为160克/摩尔).
之前,该强酸pH值与强碱pH值之间应满足的关系是____________________________. 32.(8分)下图中的每一方格表示有关的一种反应物或生成物,其中粗框表示初始反应物(反应
时加入或生成的水,以及生成沉淀J时的其他产物均已略去).
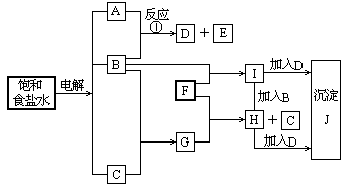 请填写下列空白:
(1)物质B是_______,F是_________,J是____________。
(2)反应①的离子方程式是_______________________。
请填写下列空白:
(1)物质B是_______,F是_________,J是____________。
(2)反应①的离子方程式是_______________________。
6摩尔/升盐酸和蒸馏水).
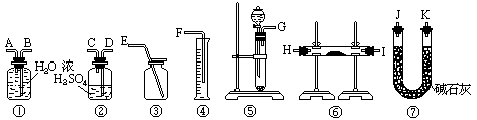 请填写下列空白:
(1)写出实验中Na2O2和Na2O分别发生反应的化学方程式_______________________________
(2)应选用的装置是(只要求写出图中装置的标号)_____________________________________。
(3)所选用装置的连接顺序应是(填各接口的字母;连接胶管省略)________________________。
请填写下列空白:
(1)写出实验中Na2O2和Na2O分别发生反应的化学方程式_______________________________
(2)应选用的装置是(只要求写出图中装置的标号)_____________________________________。
(3)所选用装置的连接顺序应是(填各接口的字母;连接胶管省略)________________________。
36.(10分)将a摩H2S和1摩O2置于一个容积可变的容器内进行反应。维持容器内气体的压强不变(101千帕),在120℃下测得反应前后容器内气体的密度分别为d1和d2。若a的取值不同,则H2S的氧化 产物可能有如下三种情况:
(1)全部是SO2,此时a的取值范围是_______。
(2)全部是S,此是a的取值范围是_______,并且d1____d2(填“小于”、“大于” 或“等于”)。
(3)部分是SO2,部分是S,此时a的取值范围是_________。反应所生成的SO2的物质的量为___摩, 容器内气体的物质的量之和为____摩。(以含a的代数式表示)
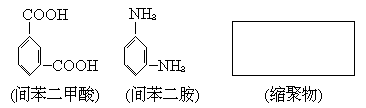
以等物质的量缩聚合成。请把Nomex纤维结构简式写在下面的方框中。
33.(8分)在有机反应中,反应物相同而条件不同,可得到不同的主产物。下式中R代表烃基,副产物均已略去。
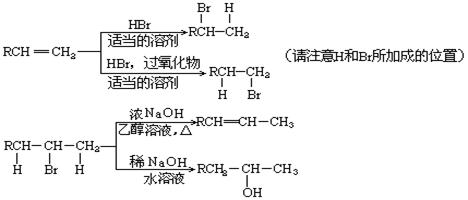
请写出实现下列转变的各步反应的化学方程式,特别注意要写明反应条件。
(1)由CH3CH2CH2CH2Br分两步转变为CH3CH2CHBrCH3
 (2)由(CH3)2CHCH=CH2分两步转变为(CH3)2CHCH2CH2OH
(2)由(CH3)2CHCH=CH2分两步转变为(CH3)2CHCH2CH2OH
(2)34.(8分)已知:
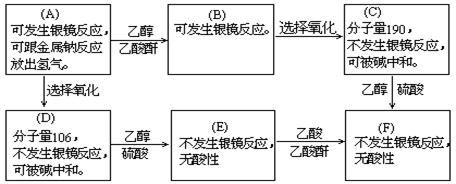 现有只含C、H、O的化合物A-F,有关它们的某些信息,已注明在下面的方框内。
现有只含C、H、O的化合物A-F,有关它们的某些信息,已注明在下面的方框内。
(1)在化合物A-F中有酯的结构的化合物是(填字母代号)。 (2)把化合物A和F的结构简式分别填入下列方框中。
 七、(本题包括2小题,共16分)
35.(6分)某化合物的化学式可表示为Co(NH3)xCly(x,y均为正整数)。为确x和 y的值,取两份质量均为0.2140克的该化合物进行如下两个实验。将一份试样溶
于水,在硝酸存在的条件下用AgNO3溶液滴定(生成AgCl沉淀),共消耗24.0毫升0.100摩/升的AgNO3溶液。在另一份试样中加入过量 NaOH溶液并加热,用足量盐酸吸收逸出的NH3。吸收NH3共消耗24.0毫升0.200摩/升HCl溶液。试 通过计算确定该化合物的化学式。
(本题可能用到的原子量:H 1.0 N 14.0 Cl 35.5 Co 58.9)
七、(本题包括2小题,共16分)
35.(6分)某化合物的化学式可表示为Co(NH3)xCly(x,y均为正整数)。为确x和 y的值,取两份质量均为0.2140克的该化合物进行如下两个实验。将一份试样溶
于水,在硝酸存在的条件下用AgNO3溶液滴定(生成AgCl沉淀),共消耗24.0毫升0.100摩/升的AgNO3溶液。在另一份试样中加入过量 NaOH溶液并加热,用足量盐酸吸收逸出的NH3。吸收NH3共消耗24.0毫升0.200摩/升HCl溶液。试 通过计算确定该化合物的化学式。
(本题可能用到的原子量:H 1.0 N 14.0 Cl 35.5 Co 58.9)
31.(6分)在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧分别进行如图所示的可逆反应。各物质的起始加入量如下:A、B和C均为4.0摩、D为6.5摩、F为2.0摩,设E为x摩。当x在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于反应器的正中位置。请填写以下空白:
(1)若x=4.5,则右侧反应在起始时向_________(填“正反应”或“逆反应”)方向进行。欲使起始反应维持向该方向进行,则x的最大取值应小于________。
(2)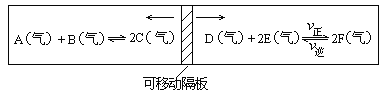 若x分别为4.5和5.0,则在
若x分别为4.5和5.0,则在
这两种情况下,当反应达平衡
时,A的物质的量是否相等?
(填“相等”、“不相等”
或“不能确定”)。其理由
是: ____________________ _______。
30.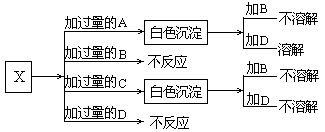 (6分)A、B、C和D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种。现利用另一种溶液X,用如下图所示的方法,即可将它们一一确定。试确定A、B、C、D、X各代表何种溶液。
A:_______ B:_______
(6分)A、B、C和D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种。现利用另一种溶液X,用如下图所示的方法,即可将它们一一确定。试确定A、B、C、D、X各代表何种溶液。
A:_______ B:_______
C:_______ D:_______
X:_______
28. (12分)在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉。这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”。请分别用下图中示意的两套仪器装置,制取上述铁的氧化物和“引火铁”。实验中必须使用普通铁粉和6摩/升盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁 圈、石棉网、加热设备等在图中均已略去)。
(12分)在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉。这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”。请分别用下图中示意的两套仪器装置,制取上述铁的氧化物和“引火铁”。实验中必须使用普通铁粉和6摩/升盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁 圈、石棉网、加热设备等在图中均已略去)。
填写下列空白: (1)实验进行时试管A中应加入的试剂是_______;烧瓶B的作用是_______;
烧瓶 C的作用是_______;在试管D中收集得到的是_______。
(2)实验时,U型管G中应加入的试剂是_______;长颈漏斗H中应加入_______。 (3)两套装置中,在实验时需要加热的仪器是_______(填该仪器对应的字母)。 (4)烧瓶I中发生的反应有时要加入少量硫酸铜溶液,其目的是_______。 (5)试管E中发生反应的化学方程式是______________。 (6)为了安全,在E管中的反应发生前,在F出口处必须______________;E管中的反应
开始后,在F出口处应_______。 五、(本题包括3小题,共16分。) 29.(4分)下图是石英晶体平面示意图,它实际上是立体的网状结构,其中硅、氧原子数
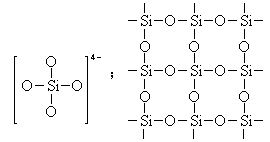 之比为____。
原硅酸根离子SiO44-的结构可表示为二聚硅酸根离子Si2O76-中,只有硅氧键,它的结构可表示为__________。
之比为____。
原硅酸根离子SiO44-的结构可表示为二聚硅酸根离子Si2O76-中,只有硅氧键,它的结构可表示为__________。
25.将pH=3的盐酸溶液和pH=11的氨水等体积混和后,溶液中离子浓度关系正确的是
(A)[NH4+]>[Cl-]>[H+]>[OH-] (B)[NH4+]>[Cl-]>[OH-]>[H+]
C)[Cl-]>[NH4+]>[H+]>[OH-] (D)[Cl-]>[NH4+]>[OH-]>[H+]
26.在一密闭容器中,用等物质的量的A和B发生如下反应:A(气)+2B(气)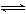 2C(气),
2C(气),
发应达到平衡 时,若混合气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率为( )。 (A)40% (B)50% (C)60% (D)70%
第Ⅱ卷 (非选择题共66分) 四、(本题包括2小题,共15分) 27.(3分)下列有关使用托盘天平的叙述,不正确的是(填写标号 )( )。
(A)称量前先调节托盘天平的零点 (B)称量时左盘放被称量物,右盘放砝码 (C)潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在
天平托盘上称量 (D)用托盘天平可以准确称量至0.01克 (E)称量完毕,应把砝码放回砝码盒中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com