
题目列表(包括答案和解析)
33.用KClO3热分解法制得的O2中常有微量的Cl2和O3,为测定Cl2和O3的含量,将KClO3分解后所得气体V1L通过足量的KI溶液,所得气体干燥后为V2L(标况),再用Na2S2O3滴定KI溶液中生成的I2,反应如下:
O3+2KI+H2O=O2+I2+2KOH ……………………①式
Cl2+2KI=I2+2KCl ……………………②式
I2+2 Na2S2O3=2NaI+ Na2S4O6 ……………………③式
若V1=1.00L,V2=0.98L,滴定时消耗0.10moL·L-1的Na2S2O3溶液0.0267L,求KClO3热分解得到的气体里Cl2和O3的体积分数。
[高三化学综合练习答案]
32.现有100mL1moL·L-1的Na2CO3溶液和100moL1.25moL·L-1的盐酸
(1)若将Na2CO3溶液逐滴加入到盐酸中,忽略CO2溶解的量,求收集到CO2的体积(标况)
(2)若将上述盐酸逐滴加入到纯碱溶液中,反应完全后,CO2在溶液中的浓度为0.04moL·L-1 ,假定溶液体积不变。求收集到CO2体积和生成物NaCl的物质的量浓度。
31.1、2-二羟基环丁烯二酮是一种强酸
(1)它的结构简式为
写出它的电离方程式_______________________________
(2)若二个氨基取代了上面化合物中的二个羟基,则变为1,2-二氨基环丁烯二酮。下面是一种叫二氯二氨合铂物质的两种异构体,一个是顺式,简称顺铂,一个是反式,简称反铂。顺铂是一种常用的抗癌药,而反式则无抗癌作用。如果用1,2-二氨基环丁烯二酮代替二个NH3与Pt结合,写出可能存在的新物质的结构简式。

___________________________________
(顺 铂) (反 铂)
30、已知CH3C-OH CH2=C=O + H2O
CH2=C=O + HCl CH2=C-Cl(极不稳定) CH3-C-Cl,从乙酸出发,
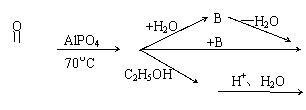 可进行如下图所示的转化
可进行如下图所示的转化
CH3-C-OH A C (C4H6O3)
D B+ ……
(1)上面的乙酸转化图中,取代反应有________________个,加成反应有_________个,消去反应有________________个。
(2)C.D的结构简式为:C _______________D________________
 (3)C的同分异构体甚多,其中含一个-OH的四元环(三个C、一个O构成)的环酯化合物有_________________个。
(3)C的同分异构体甚多,其中含一个-OH的四元环(三个C、一个O构成)的环酯化合物有_________________个。
29、有甲、乙、丙三种常见单质,在下列反应流程中转化为X、Y、Z三种常见的化合物:

 O2
O2
 充分燃烧
充分燃烧
(1)在X、Y、Z中一定含有乙元素的有________________________
(2)单质乙是无色气体,它的化学式______________理由是______________________
(3)X、Y、Z的组成(写化学式)可能有二组,它们分别是
 ①________________________②_______________________
①________________________②_______________________
28、重铭酸钾化学式为K2Cr2O7,俗称红矾,有毒。它是可溶性的美丽的红色晶体,将K2Cr2O7跟浓H2SO4混合,发生反应:K2Cr2O7 + H2SO4 == K2SO4 + 2CrO3 + H2O,得到的CrO3是橙红色晶体,与水反应得到红色的溶液。它能将铜件表面处理得很光亮且不易锈蚀。
(1)生成CrO3的反应是由两种基本类型的反应共同完成的,一种是____________反应,另一种是__________反应。
(2)CrO3属于哪一类氧化物_______________
(3)将CrO3的水溶液与过量NaOH反应时,可得到一种类似硫酸钠组成的的黄色盐类,它的化学式为__________________.
27、在NaNO2中N元素的化合价为+3价,为证明和研究NaNO2的性质,现有以下几种试剂可供选择:
①KMnO4溶液 ②稀H2SO4 ③稀HNO3 ④稀NaOH溶液
⑤淀粉-KI溶液 ⑥品红溶液
(1)证明NaNO2具有还原性应选择的试剂是______反应的离子方程式为________________
(2)证明NaNO2具有氧化性应选择的试剂是________________反应过程中观察到的实验现象是___________________
(3)在NaNO2溶液中加入稀硫酸时,溶液出现浅蓝色,这说明生成的新物质是_____________,表示这一反应的化学方程式是__________________________
26、实验室用草酸标定氢氧化钠溶液的准确浓度,达到滴定终点时,用酚酞试液作指标剂显浅红色,化学方程式为
 H2C2O4 + 2NaOH
Na2C2O4
+ 2H2O
H2C2O4 + 2NaOH
Na2C2O4
+ 2H2O
(1)某学生在用此法测定NaOH溶液浓度的全过程为:
A、为配制0.100mol·L-1的草酸溶液,用电子天平称取H2C2O4·2H2O 1.260g
B、将晶体放入一个500mL的大烧杯中,用蒸馏水溶解,冷至室温
C、将溶液转移至100mL容量瓶中,并洗涤2次,也转移至容量瓶中
D、继续向容量瓶加水,接近标线约2cm时,改用胶头滴管加水至标线
E、反复振荡容量瓶,摇匀。
F、将碱式滴定管用蒸馏水洗3次后注入待测的NaOH溶液
G、调节滴定管液而高度在“0”或“0”刻度以下,同时赶走尖嘴气泡
H、取一锥形瓶,用标准草酸溶液润洗2次,加入20.00mL草酸溶液
I、加入酚酞后滴定,当锥形瓶内溶液颜色由无色至浅红色,且半分钟不褪,滴定终点。
J、根据记录初读数和终读数,NaOH溶液用去23.01mL
指出上述实验过程中的错误之处(填编号)__________________________
(2)另一学生同做该实验,记录有关数据如下:
|
实验次数编号 |
草酸溶液体积V/mL |
NaOH溶液体积V/mL |
|
1 |
20.00 |
21.47 |
|
2 |
20.00 |
20.96 |
|
3 |
20.00 |
24.77 |
|
4 |
20.00 |
21.32 |
根据该学生所做实验,请分析NaOH溶液浓度取值合理的是__________________
A、0.0904mol·L-1 B、0.081mol·L-1 C、0.0941mol·L-1 D、0.1880mol·L-1
25、已知CuSO4在25℃时的溶液为25g,在此温度下,将50gCuSO4加入100g水中充分搅拌溶解后,所得溶液质量为
A、83.64g B、104.55g C、114.6g D、125g
24、用两支惰性电极插入1000mL CuSO4溶液,通电电解,当电解液的PH由6.0变为3.0时,下列叙述正确的是
A、阳极上析出1×10-3L氧气(标况) B、阴极上析出32mg铜
C、阳极和阴极质量都没有变化 D、阴极上析出11.2mL氢气(标况)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com