
题目列表(包括答案和解析)
4、引入摩尔的意义:摩尔象一座桥梁把单个的肉眼看不见的微粒跟很大数量的微粒集体,可称量的物质之间联系起来。
例:化合物E(含二种元素)与氨气反应,生成化合物G和H2,化合物G的式量约为81,G分子中硼元素,(B原子量为10.8)和氢元素的质量分数分别是0.40和0.074,由此推断:(1)化合物G的化学式为___________________
(2)反应消耗1molNH3,可生成2molH2,则组成化合物E的元素是_____和_____
(3)1molE和2molNH3恰好完全反应,化合物E的化学式为_________________
解析:(1)由E+NH3→G+H2可知,G中必含N元素,则1molG中含B、H、N的物质的量分别为:B: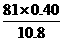 =3,H:
=3,H: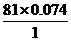 =6,N:
=6,N: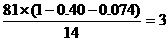
则G的化学式为B3N3H6即所谓的无机苯。
(2)同样由E+NH3→G+H2可知,由于G中含B元素,则E中必含B元素,(NH3中无B元素)而每消耗1molNH3(只含3molH原子)则可生成2molH2,(含4molH原子),由H原子守恒可知,E中必含氢元素,即E由B和H两种元素组成。
(3)据题意:1molE恰好和2molNH3反应,应理解为E和NH3按nE: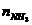 =1:2的物质的量比反应,因为E+2NH3--G(B3N3H6)+H2,反应前后N原子必相等,则NH3的计量系数至少为6,而B3N3H6的计量系数应为2,则E的计量系数应为3(nE:
=1:2的物质的量比反应,因为E+2NH3--G(B3N3H6)+H2,反应前后N原子必相等,则NH3的计量系数至少为6,而B3N3H6的计量系数应为2,则E的计量系数应为3(nE: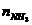 =1:2)又由于1molNH3反应可生成2molH2(题(2)中的条件应继续运用),则6molNH3应生成12molH2,即反应式为3E+6NH3=2B3N3H6+12H2,由B原子守恒,1molE应含2molB,再由H原子守恒,1molE应含6molH原子,即E的化学式为B2H6(即所谓乙硼烷)。从本题的解析过程应看出:解此类习题一是要充分运用化学反应中各物质的计量关系,熟练运用摩尔、质量守恒定律的知识;二是认真审题,充分利用题设条件,特别是在解答下一问时要注意到上一间所提供的条件。
=1:2)又由于1molNH3反应可生成2molH2(题(2)中的条件应继续运用),则6molNH3应生成12molH2,即反应式为3E+6NH3=2B3N3H6+12H2,由B原子守恒,1molE应含2molB,再由H原子守恒,1molE应含6molH原子,即E的化学式为B2H6(即所谓乙硼烷)。从本题的解析过程应看出:解此类习题一是要充分运用化学反应中各物质的计量关系,熟练运用摩尔、质量守恒定律的知识;二是认真审题,充分利用题设条件,特别是在解答下一问时要注意到上一间所提供的条件。
3、摩尔质量--单位物质的量的物质所具有的质量,即M= 显然摩
显然摩
尔质量与1mol物质的质量意义不同,只不过数值相同,且等于其式量。单位不同,一个是g·mol-1,而另一个是g。
2、阿伏加德罗常数就是12gC12所含碳原子数,由此可以看出:
(1)阿伏加德罗常数是一个精确值(12gC-12含碳的原子数是个定值)
(2)阿伏加德罗常数可通过实验测定
(3)6.02×1023是个非常近似的值。
1、物质的量物理意义:衡量宏观物质的质量和微观粒子数量的物理量,它是七个国际
单位制物理量中的一个(质量、长度、时间、电流强度、热力学温度、光学强度)。其单位是摩尔。
26.(12分)将10克铁粉置于40mL硝酸中,再微热,反应过程随着硝酸浓度的降低,生成
气体的颜色由红棕色逐渐变为无色,充分反应后,共收集到1.792L混合气体(标准状况),
此时溶液中还残留4.4克固体。
(1)求该反应中被还原的硝酸和未被还原的硝酸的质量比;
(2)求原硝酸溶液的物质的量浓度;
(3)求混合气体中NO和NO2的体积比。
4.24g。另取一定质量的此混合物固体,跟100mL某浓度的盐酸刚好完全反应,并收集
到 672mLCO2气体(标准状况下)求:
(1)此混合物中NaHCO3的质量百分含量;
(2)所用盐酸的物质的量浓度。
25.(7分)将Na2CO3和NaHCO3的混合物5.48g加热到质量不再减轻时,测得残留固体
24.(10分)2,4,5-三氯苯酚和氯乙酸反应可制得除草剂2,4,5-三氯苯氧乙酸。某生
产该除草剂的工厂在一次事故中泄漏出一种二恶英,简称为
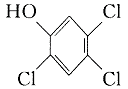 TCDD。有关物质的结构式如下:
TCDD。有关物质的结构式如下:
三氯苯酚 氯乙酸Cl-CH2COOH
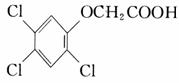
请写出:
|
反应的化学方程式:
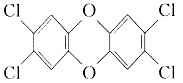
(2)(4分)2,4,5-三氯苯酚生成TCDD
反应的化学方程式 。
23.(10分)在某些酶的催化下,人体内葡萄糖的代谢有如下过程:
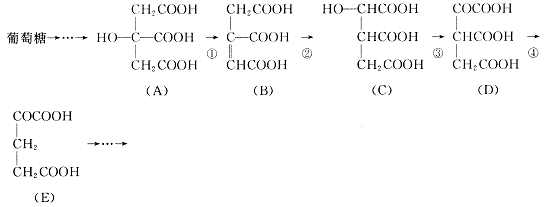
请填空:
(1)过程①是 反应,过程②是 反应,过程③是 反
应(填写反应类型的名称)。
(2)过程④的另一种生成物是 (填写化学式)。
(3)上述物质中 和 互为同分异构体(填写字母代号)
22.(10分)氯酸是一种强酸,氯酸的浓度超过40%,就会迅速分解,产生比它的酸性更强
的酸,同时放出气体,该气体混合物经干燥后,平均分子量为47.6,它可以使带火星的
木条复燃,并可使润湿的淀粉碘化钾试纸变蓝后又褪色,试完成下列各题:
(1)该气体的组成是______________气体混合物的物质的量比为__________________
(2)写出氯酸分解方程式并配平该反应的还原产物是__________________。
(3)结合化学方程式解释,该气体使润湿的淀粉碘化钾试纸变蓝后又褪色的原因。
___ ______________________________________________________
___ ______________________________________________________
___ ______________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com