
题目列表(包括答案和解析)
10. 对于反应 4NH3(g)+5O2(g)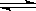 4NO(g)+6H2O(g) (正反应为放热反应),下列有关叙述正确的是( )
4NO(g)+6H2O(g) (正反应为放热反应),下列有关叙述正确的是( )
A.若降低温度,达到新的化学平衡时,NO的体积分数将增大
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.对NH3与O2的反应来说,化学反应速率关系是2υ(NH3)=3υ(H2O)
9.一种离子与多种酸根离子构成的盐称为“混盐”,如氯化硝酸钙[Ca(NO3)Cl];而复盐是指含有多种简单阳离子和一种酸根离子的盐,如KAl(SO4)2,据此,下列各化合物中属于混盐的是( )
A.(NH4)2Fe(SO4)2 B.CaOCl2
C. BiONO3 D.K3[Fe(CN)6]
8. 某种氯化镁晶体有24Mg2+、35Cl-、37Cl-、三种离子组成,在熔融状态下,使1mol这种氯化镁完全电解,测得产生的气体质量为同体积氧气质量的2.22倍。则这种氯化镁晶体中35Cl-与37Cl-与的物质的量之比为( )
A.1:2 B.2:3 C.1:3 D.3:1
7. 1
mol有机物  与足量NaOH 溶液充分反应,消耗NaOH 物质的量为( )
与足量NaOH 溶液充分反应,消耗NaOH 物质的量为( )
A.5 mol B.4 mol C.3 mol D.2 mol
6.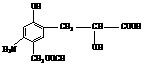 分析有机物的结构
分析有机物的结构
应具有的性质是:( )
① 缩聚反应 ②加成反应 ③取代反应 ④水解反应 ⑤中和反应 ⑥显色反应 ⑦氧化反应 ⑧还原反应 ⑨消去反应
A.只③⑤⑥⑦ B.只④⑤⑥⑦
C.全部 D.除①④外其余都有
5.在容器中充入SO2和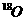 2,在一定条件下反应达到平衡时,SO2中的
2,在一定条件下反应达到平衡时,SO2中的 含量与平衡前相比将( )
含量与平衡前相比将( )
A.下降 B.不变 C.增大 D.不能确定
4. 在体积可变的密闭容器中建立氨气在水中的溶解平衡和电离平衡,在右图的容器中按图示操作,下列各项叙述正确的是 ( )
在体积可变的密闭容器中建立氨气在水中的溶解平衡和电离平衡,在右图的容器中按图示操作,下列各项叙述正确的是 ( )
A.氨水的浓度增大,pH减小
B.液面上氨气的压强增大,水溶液的pH不变
C.液面上氨气的压强不变,溶液的浓度增大,pH变大
D.液面上氨气的压强变大,溶液的浓度增大,NH3·H2O电离度变大
3.明矾的主要成分是KAl(SO4)2·12H2O,关于明矾的下列说法不正确的是
 A.电离方程式为:KAl(SO4)2 K++Al3++2SO
A.电离方程式为:KAl(SO4)2 K++Al3++2SO
B.可以做食品的膨化剂
C.能净化水,但不能使硬水软化
D.明矾中有Al3+,多食对人体健康不利
2.工矿企业必须严格执行关于“三废”排放标准,并且尽可能地把“三废”变成有用的副产品,否则将会严重地污染环境。下列有关工业生产中的“三废”因任意排放,可能导致“光化学污染”的是( )
A.硫酸工业废气 B.工业生产硝酸的尾气
C.工业电镀锌的废水 D.火力发电厂的废渣
1.某矿泉水标签上印有主要的矿物质成分如下(单位mg/L):Ca 20, K 39 , Mg 3.0 Zn 0.06 , F 0.02 等。这里的Ca、K、Mg、Zn、F是指( )
A.单质 B.元素 C.金属离子 D.分子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com