
题目列表(包括答案和解析)
3、下列关于乙酸乙酯的各种说法中正确的是( )
A、酯化时需要用水浴加热,才可进行
B、乙酸乙酯中含有乙酸时,可用NaOH溶液除去
C、乙酸乙酯是一种优良的溶剂
D、酯化反应中,酸羟基中的18O原子在产物酯中
2、实验室制备下列物质时,不可用浓H2SO4参与的是( )
 A、由 制取硝基苯
B、用乙酸和乙醇制备乙酸乙酯
A、由 制取硝基苯
B、用乙酸和乙醇制备乙酸乙酯
C、用NaI制HI D、由乙醇制乙烯
1、下列物质,不属于运输中易燃易爆危险品的是( )
A、三硝基甲苯 B、酚醛塑料 C、三硝基苯酚 D、乙醛
|
|

|
|
 盖尔达法:蛋白质
硫酸铵
氨
盖尔达法:蛋白质
硫酸铵
氨
求:(1)30.0mL牛奶中含有多少克氮?
(2)如果蛋白质中氮元素的质量分数为16.8%,则牛奶中含蛋白质的质量分数为多 少?
25.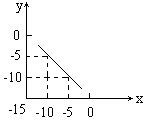 (8分)某温度下的溶液中,c(H+)=10x mol/L,c(OH-)=10y
mol/L。x与y的关系如右图所示;
(8分)某温度下的溶液中,c(H+)=10x mol/L,c(OH-)=10y
mol/L。x与y的关系如右图所示;
(1)求该温度下,中性溶液的pH。
(2)求该温度下0.01mol/L NaOH溶液的pH。
(3)该温度下,pH= a的醋酸溶液与pH= b的NaOH溶液等体积混合,恰好完全反应,求此醋酸溶液中醋酸的电离度。
高考科目教学质量第一次检测
|
(1)写出实验室制乙烯的化学反应方程式 。
(2)下表中有左右两栏,左栏中有一项跟右栏中四项相关,把左栏中的这一项和右栏中根本不相关的一项选出。
|
左栏 |
右栏 |
|
A.葡萄糖 B.蔗糖 C.淀粉 |
①混合物 ②有甜味 ③没有还原性 ④能发生水解反应 ⑤高分子化合物 |
|
|
答案:左栏 右栏 。
23. (11分)有机物A的结构简式为
(11分)有机物A的结构简式为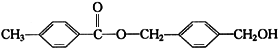 ,从A出发,可发生图示中的一系列反应。其中K的分子式为C12H14O4,L和K互为同分异构体,F的产量可作为衡量一个国家石油化工发展水平的标志。(图中[O]表示氧化)
,从A出发,可发生图示中的一系列反应。其中K的分子式为C12H14O4,L和K互为同分异构体,F的产量可作为衡量一个国家石油化工发展水平的标志。(图中[O]表示氧化)
已知甲苯经氧化可生成苯甲酸:
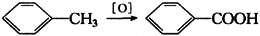
请写出:
(1)下列物质的结构简式
|
|
|
|
C+J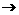 L
。
L
。
|
21.(11分)实验室用稀硝酸与铜反应来制备NO气体,如果采用(Ⅰ)装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不十分理想,因为从观察到的现象不能有力证明反应产物是NO;有人设计了(Ⅱ)装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果。

|
|
|
①将分液漏斗的活塞打开,从U型管的B侧管口注入稀硝酸,一直注到 为止。
|
|
|
②如果再将分液漏斗的活塞慢慢打开,可立即观察到哪些明显现象?
18.(6分)有A、B、C、D、E、F六种短周期的主族元素,原子序数依次增大,其中A、D元素的原子最外电子层均只有一个电子,且A和D可形成离子化合物;C、F同主族,B元素位于元素周期表中第二周期,且原子最外层电子数占核外电子总数的3/4,F元素原子最外电子层比同周期的E元素原子的最外电子层多5个电子。
|
|
|
(3)D的氢氧化物和C的氢化物在水溶液中反应的离子方程式为 。
|
|
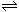 B (g),在一定条件下达到平衡,在温度不变时,改变下列条件时,请判断气体A的平衡浓度c(A)和气体B的平衡浓度c(B)的比值
B (g),在一定条件下达到平衡,在温度不变时,改变下列条件时,请判断气体A的平衡浓度c(A)和气体B的平衡浓度c(B)的比值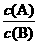 的变化情况,在小题后括号内填“增大”、“减小”或“不变”。
的变化情况,在小题后括号内填“增大”、“减小”或“不变”。
|
|
|
17.(6分)在一定条件下可实现下列物质间的转化,如下图所示:
|

|
(2)工业上曾利用C来制取B,在制取过程中还需加入一种 物质(填该物质的化学式)。
|
16.已知HIO既能和酸又能和碱发生中和反应,则它与盐酸反应的产物是
A. IO- B. H2O C. HI D. ICl
15.某溶液中含有大量Fe2+、Fe3+、Mg2+和NH4+,其c(H+)=10-2mol·L-1,在该溶液中可以大量存在的阴离子是
A. SO42- B. NO3- C. I- D. CO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com