
题目列表(包括答案和解析)
16、NH3分子与H+间以 键结合成NH4+的过程可用电子式表示为: 。
15、 镭(Ra)位于周期表的第七周期ⅡA族。下列关于镭的性质的描述不正确的是
A. 在化合物中呈+2价 B. 单质能使水分解产生氢气
C. 氢氧化物呈两性 D. 碳酸盐难溶于水
14、正电子、反质子等都属于反粒子,它们跟普通电子、质子的质量、电量均相等,而电性相反。科学家设想在宇宙的某些区域可能存在完全由反粒子构成的物质--反物质。1998年初和年底,欧洲和美国的科研机构先后宣布:他们分别制造出9个和7个反氢原子,这是人类探索反物质的一大进步。你推测反氢原子是:
A 由1个带正电的质子和1个带负电的电子构成
B 由1个带负电的质子和1个带正电的电子构成
C 由1个不带电的中子和1个带负电荷的电子构成
D 由1个带负电荷的质子和1个带负电荷的电子构成
13、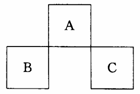 A、B、C均为短周期元素,它们在周期表中的位置如左图所示。
A、B、C均为短周期元素,它们在周期表中的位置如左图所示。
已知:B、C两元素原子最外层电子数之和等于A元素原子最外层电子数的2倍;B、C两元素的核电荷数之和是A元素原子序数的4倍。则A、B、C分别是
A C、Al、P B N、Si、S C 0、P、Cl D F、S、Ar
12、许多物质在通常条件下是以晶体的形式存在,而一种晶体又可视作若干相同的基本结构单元构成,这些基本结构单元在结构化学中被称作晶胞。已知某化合物是由钙、钛、氧三种元素组成的晶体,其晶胞结构如图所示,则该物质的化学式为
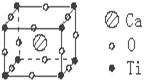
A.Ca4TiO3 B.Ca4TiO6
C.CaTiO3 D.Ca8TiO12
11、第3周期元素R,它的原子核外最外层上达到饱和所需电子数小于次外层和最内层电子数之差,且等于最内层电子数的正整数倍。则关于R的正确说法是
A 常温下,能稳定存在的R的高价氧化物都能与烧碱溶液反应
B R的最高价氧化物对应水化物是强酸
C R和R的氧化物的熔点和硬度都很高
D R能形成稳定的气态氢化物
10、短周期元素A、B、C原子序数依次递增,它们的原子的最外层电子数之和为10。A与C在周期表中同主族,B原子最外层电子数等于A原子次外层电子数。下列叙述正确的是
A 原子半径A<B<C B A的氢化物的稳定性大于C的氢化物
C B的氢化物的熔点比A氧化物高 D A与C可形成离子化合物
9、下列过程中,共价键被破坏的是
A.碘升华 B.溴蒸气被木炭吸附
C.NaCl溶于水 D.HCl气体溶于水
8、下列排列顺序错误的是
A、金属性 Rb>K>Mg>Al B、非金属性 As>S>Cl>F
C、稳定性 AsH3>PH3>H2S>HF D、半径 Na>P>O>F
7、近来查明,二氧化三碳(C3O2)是金星大气层的一个组成部分,下列关于二氧化三碳的说法错误的是 .. ..
A、二氧化三碳的电子式为 :O::C::C::C::O: B、C3O2、CO、CO2都是碳的氧化物
C、C3O2和CO一样可以燃烧生成CO2 D、C3O2和CO2都是碳酸的酸酐
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com