
题目列表(包括答案和解析)
5.为除去镀在铝表面的铜镀层可选用的试剂是
A.稀硝酸 B.浓硝酸
C.浓硫酸 D.浓盐酸
4.现有下列物质:①氯水,②氨水,③浓硝酸,④氢氧化钠,⑤液溴。其中必须保存在棕色瓶里的是
A.全部 B.①③⑤
C.只有①③ D.①②④
3.硝酸与各种金属单质反应时,一般不会生成的物质是
A.NO B.NO2
C.NH4NO3 D.H2
2.久置的浓硝酸往往显黄色,其原因是
A.溶有Fe3+ B.溶有Br2
C.溶有NO2 D.溶有有机色素
1.(2002年全国高考题)化合价为n的某元素的硝酸盐的式量为x,其氢氧化物的式量为y,则n的值是
A.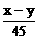 B.
B.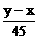
C.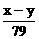 D.
D.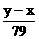
14.(18分)现有一份“将二氧化硫转化为硫酸铵”的资料,摘录如下:
一个典型实例:初步处理后的废气含0.20%的二氧化硫和10%的氧气(体积分数)。在
400℃时废气以5 m3·h-1的速率通过五氧化二钒催化剂层与20 L·h-1的速率的氨气混合,再喷水,此时气体温度由400℃降至200℃,在热的结晶装置中得到硫酸铵晶体(气体体积均已折算为标准状况)。
利用上述资料,用氨来除去工业废气中的二氧化硫,回答下列问题:
(1)按反应中的理论值,二氧化硫和氧气的物质的量之比为2∶1,该资料中这个比值是 ,简述不采用2∶1的理由是 。
(2)通过计算,说明为什么废气以5 m3·h-1的速率与20 L·h-1速率的氨气混合?
(3)若某厂每天排放1×104 m3这种废气,按上述方法该厂每月(按30天计)可得硫酸铵多少吨?消耗氨气多少吨?
13.(12分)可逆反应aA(g)+bB(g) cC(g)+dD(g),取a mol A和b mol B置于V L容器中,1
min后,测得容器内A的浓度为x mol·L-1,这时B的浓度为 mol·
cC(g)+dD(g),取a mol A和b mol B置于V L容器中,1
min后,测得容器内A的浓度为x mol·L-1,这时B的浓度为 mol·
L-1,C的浓度为 mol·L-1。这段时间内反应的平均速率若以物质A的浓度变化来表示,应为 。
12.(5分)反应A+3B==2C+2D在四种不同情况下的反应速率分别为①v(A)=0.15 mol·L-1·s-1;②v(B)=0.6mol·L-1·s-1;③v(C)=0.4 mol·L-1·s-1;④v(D)=0.45 mol·L-1·s-1。该反应进行的快慢顺序为 。
11.(8分)根据化学方程式2N2O 2N2+O2,填充表中①、②、③、④空栏处测定反应速率的实验数据和计算结果。
2N2+O2,填充表中①、②、③、④空栏处测定反应速率的实验数据和计算结果。
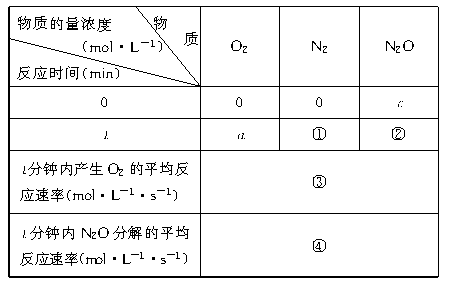
①
②
③
④
10.(12分)(2001年上海高考题)某化学反应2A B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
|
实验 序号 |
时间 浓度 温度 |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
|
2 |
800℃ |
C2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
|
3 |
800℃ |
C3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
|
4 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20 min时间内平均速率为 mol·(L·min)-1。
(2)在实验2中A的初始浓度C2= mol·L-1,反应经20 min就达到平衡,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3 v1?(填“>”“=”或“<”=,且C3 1.0 mol·L-1(填“>”“=”或“<”=。
(4)比较实验4和实验1,可推测该反应是 反应(选填“吸热”或“放热”)。理由是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com