
题目列表(包括答案和解析)
16.在含有Cu(NO3)2、Fe(NO3)3、AgNO3各0.1mol的混合溶液中,加入铁粉,经反应后未见气体放出,当析出3.2gCu时,溶解的铁粉的质量是
A.2.8g B.5.6g C.8.4g D.14g
第Ⅱ卷(非选择题,共60分)
15.五氧化二氮是白色固体,熔点为30℃,升温时易液化和气化,并发生以下两个相互联系的反应:①N2O5(g) N2O3(g)+O2(g);②N2O3(g)
N2O3(g)+O2(g);②N2O3(g) N2O(g)+O2(g)。在0.5L密闭溶器中,将2.5mol N2O5加热气化,并按上述①②两式分解,在某温度下达到平衡,测得O2的平衡浓度为4.4mol·L-1,N2O3的平衡浓度为1.6mol·L-1,则下列各项判断正确的是:
N2O(g)+O2(g)。在0.5L密闭溶器中,将2.5mol N2O5加热气化,并按上述①②两式分解,在某温度下达到平衡,测得O2的平衡浓度为4.4mol·L-1,N2O3的平衡浓度为1.6mol·L-1,则下列各项判断正确的是:
A.N2O5的平衡浓度为3.0mol·L-1 B.N2O5的转化率为60%
C.平衡时N2O3的物质的量为0.7mol D.N2O的平衡浓度为4.4mol·L-1
14.电解含有重水(D2O)的普通水时,在两极共收集到气体18.5 g,其体积恰好是33.6L(标准状况)。这些气体中普通氢和重氢(D)的原子个数比为
A.1︰1 B.2︰1 C.3︰1 D .4︰1
13.下列反应的离子方程式书写正确的是
A.氯化铁溶液中通入SO2气体 Fe3+ +SO2 +2H2O = Fe2+ +SO42- + 4H+
B.Na2CO3溶液中滴加盐酸至刚好出现气泡时停止 CO32-+2H+ = CO2↑+H2O
C.向烧碱溶液中通入少量SO2气体 SO2+OH-=HSO3-
D.向Ba(OH)2溶液中逐滴加入NH4HSO4至刚好沉淀完全
Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+H2O
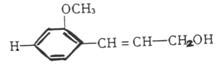
12. 从松树中分离出松柏醇,其结构简式为:
下列叙述正确的是
A.它难溶于水,也不溶于有机溶剂
B.1mol该化合物最多能与4molH2发生加成反应
C.它不溶于NaHCO3溶液,但可与NaOH溶液发生中和反应
D.1mol该化合物在溴水中最多能与4molBr2发生加成反应
11.下列可用相同的方法除去混有的杂质的是
A.Fe(OH)3胶体中混有少量NaCl及盐酸,淀粉溶液中混有少量KI
B.淀粉溶液中混有少量NaCl,蔗糖中混有少量NaCl
 C.Na2CO3中混有少量NaHCO3、NaHCO3中混有少量Na2CO3
C.Na2CO3中混有少量NaHCO3、NaHCO3中混有少量Na2CO3
D.铁粉中混有少量硫粉,碘中混有NaCl
10.第3周期元素R,它的原子核外最外层上达到饱和所需电子数小于次外层和最内层电子数之差,且等于最内层电子数的正整数倍。则关于R的正确说法是
A.R能形成稳定的气态氢化物
B.R的最高价氧化物对应水化物是强酸
C.R和R的氧化物的熔点和硬度都很高
D.常温下,能稳定存在的R的高价氧化物都能与烧碱溶液反应
9.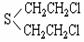 黑龙江省齐齐哈尔市2003年8月4日发生一起侵华日军遗弃化学毒剂芥子气泄漏致多人受伤事件。芥子气学名为“二氯二乙硫醚”,被称为“毒气之王”,结构见下图,它为无色油状液体,工业品呈棕褐色,有大蒜气味,沸点219℃,液体密度1.27g/cm-3;难溶于水,易溶于有机溶剂(汽油、煤油、酒精),能溶于动植脂肪中;常温水解极慢,加热能使水解加快;能与高锰酸钾、漂白粉及硫化钠溶液反应。战争使用状态为液滴态或雾状。下列有关芥子气的叙述正确的是
黑龙江省齐齐哈尔市2003年8月4日发生一起侵华日军遗弃化学毒剂芥子气泄漏致多人受伤事件。芥子气学名为“二氯二乙硫醚”,被称为“毒气之王”,结构见下图,它为无色油状液体,工业品呈棕褐色,有大蒜气味,沸点219℃,液体密度1.27g/cm-3;难溶于水,易溶于有机溶剂(汽油、煤油、酒精),能溶于动植脂肪中;常温水解极慢,加热能使水解加快;能与高锰酸钾、漂白粉及硫化钠溶液反应。战争使用状态为液滴态或雾状。下列有关芥子气的叙述正确的是
A.它能水解生成二羟二乙硫醚 B.化学性质不稳定,易分解
C. 中毒后使细胞组织坏死、糜烂,但能较快愈合 D.常温下它易挥发
8.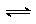 Fe(NO3)2溶液呈浅绿色,其中存在下列平衡:Fe2++2H2O Fe(OH)2+2H+,往该溶液逐滴加入盐酸,发生的变化是 (已知3Fe2++4H++NO3-=3Fe3++NO↑+2H2O)
Fe(NO3)2溶液呈浅绿色,其中存在下列平衡:Fe2++2H2O Fe(OH)2+2H+,往该溶液逐滴加入盐酸,发生的变化是 (已知3Fe2++4H++NO3-=3Fe3++NO↑+2H2O)
A.平衡不移动 B.平衡向正方向移动
C.溶液颜色由浅绿色变为棕黄色 D.溶液颜色由浅绿色变为深绿色
7.正电子、反质子等都属于反粒子,它们跟普通电子、质子的质量、电量均相等,而电性相反。科学家设想在宇宙的某些区域可能存在完全由反粒子构成的物质--反物质。1998年初和年底,欧洲和美国的科研机构先后宣布:他们分别制造出9个和7个反氢原子,这是人类探索反物质的一大进步。你推测反氢原子是:
A.由1个带正电的质子和1个带负电的电子构成
B.由1个带负电的质子和1个带正电的电子构成
C.由1个不带电的中子和1个带负电荷的电子构成
D.由1个带负电荷的质子和1个带负电荷的电子构成
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com