
题目列表(包括答案和解析)
1、随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是( )。
A、利用电池外壳的金属材料 B、不使电池中渗泄的电解液腐蚀其他物品
C、防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 D、回收其中的石墨电极
25.(8分)往400mL 0.3mol/L NaOH溶液中通入一定量的CO2气体,然后在低温下蒸发溶液,得白色固体A为7.6g。试推算:
(1)A的可能成分;
(2)组成A的物质的质量;
(3)求通入的CO2气体在标准状态下的体积。
24.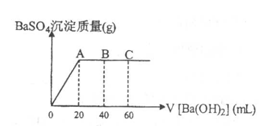 (5分)t℃时,稀硫酸和盐酸混合溶液中c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知a+b=12。向20mL该混合酸溶液中逐滴加入pH=11的Ba(OH)2溶液,生成BaSO4的量如图所示,当加入60mL Ba(OH)2溶液时,C点溶液的pH=6(体积变化忽略不计),试计算:
(5分)t℃时,稀硫酸和盐酸混合溶液中c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知a+b=12。向20mL该混合酸溶液中逐滴加入pH=11的Ba(OH)2溶液,生成BaSO4的量如图所示,当加入60mL Ba(OH)2溶液时,C点溶液的pH=6(体积变化忽略不计),试计算:
(1)最初混合酸溶液中:
c(H2SO4)= ▲ ,c(HCl)=___ ▲____;
(2)A点的pH=_____▲____;
(3)B点比最初混合酸的pH增加多少(写出计算过程)?(lg3=0.48)
23.(7分)工业上可用乙基醌经两步反应制备H2O2,其工艺流程可简单表示如下:

(1)涉及还原反应的方程式可写成 ▲ ,
涉及氧化反应的方程式可写成 ▲ 。
(2)“绿色化学”是当今社会人们提出一个新概念,“绿色化学”工艺中原子利用率为100%,不产生副产物。试问该法生产H2O2可否成为理想状态的“绿色化学”工艺? ▲ (填“是”或“不是”),并简述理由 ▲ 。
22.(3分)与甲酸的相对分子质量相差14,但不是甲酸同系物的有机物的结构简式为
▲ 、 ▲ 、 ▲ 。
21.(12分)实验室里临时需要用NaOH溶液和CO2来制取纯Na2CO3溶液。已知CO2气体在通入NaOH溶液过程中极易过量生成NaHCO3,且无明显现象。
实验室有下列试剂:①未知浓度的NaOH溶液;②37%的盐酸;③37%的硫酸; ④14%的盐酸;⑤大理石;⑥K2CO3固体;⑦Cu2(OH)2CO3。
实验室有下列仪器:铁架台、启普发生器、量筒、烧杯、橡皮管、玻璃导管、分液漏斗。
已知下表中各物质在常温时的溶解度(g/100g H2O)
|
Na2CO3 |
NaHCO3 |
NaCl |
Na2SO4 |
NaHSO4 |
NaOH |
|
15.9 |
8.4 |
35.0 |
35.5 |
20.0 |
40.0 |
(1)本实验应选用的仪器:除烧杯、量筒、橡皮管、玻璃导管外,还需要 ▲ ;
(2)为保证制得的Na2CO3溶液尽量纯,应选用的药品(写编号):除①外,还需要
▲ ;
(3)简要叙述实验步骤,直到制得纯Na2CO3溶液(仪器安装可省略):
▲ ;
(4)根据给出的溶解度表,求出当NaOH溶液中溶质的质量分数大于多少时,在配制过程中有晶体析出(写出计算步骤和必要的文字说明) ▲ 。
20.(5分)下面a-e是中学化学实验中常见的几种定量仪器:
a. 量筒、b. 容量瓶、c. 滴定管、d. 托盘天平、e. 温度计。
(1) 其中标有“0”刻度,且“0”刻度在上方的仪器是 ▲ (填编号);
(2) 能够用以精确量取液体体积的是 ▲ (填写编号);
(3) 由于错误操作, 使得到的数据比正确数据偏小的是 ▲ (填写编号):
A. 用量筒量取液体时, 俯视液面读量取体积;
B.中和滴定达终点时,俯视液面读数,计算消耗溶液体积;
C.用容量瓶配制一定物质的量浓度溶液, 定容时俯视液面所配得溶液浓度;
(4) 有下列实验:①苯与溴的取代反应,②苯的硝化反应,③乙醛的银镜反应,④石油分馏实验,⑤乙酸乙酯的制取。其中需要使用温度计的有 ▲ (填写编号)。
19.(5分)在10.0℃和2×105Pa的条件下,aA(g)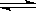 dD(g)+eE(g) 建立平衡后,再逐步增加体系的压强(温度维持不变),下表列出了不同压强下反应建立平衡时物质D的浓度:
dD(g)+eE(g) 建立平衡后,再逐步增加体系的压强(温度维持不变),下表列出了不同压强下反应建立平衡时物质D的浓度:
|
压强(Pa) |
2×105 |
5×105 |
1×106 |
|
D的浓度(摩/升) |
0.085 |
0.20 |
0.44 |
据表中数据,可见压强从2×105 Pa增至5×105 Pa,平衡向 ▲ 方向移动,作出这种判断的理由是 ▲ ;当压强由5×105 Pa增加到1×106 Pa时,平衡向 ▲ 方向移动, 作出这种判断的理由是
▲ ,平衡之所以向该方向移动,这是由于 ▲ 。
18.(9分)固体A的化学式为NH5,它的所有原子的最外层都符合相应的稀有气体原子电子层结构,该物质适当加热就分解成两种气体,试回答:
(1)固体A属于 ▲ 晶体,它的电子式为 ▲ ;
(2)A溶于水后溶液呈 ▲ 性(填“酸”、“碱”或“中”),其原因是(用化学方程式表示) ▲ ;
(3)A与铜或铜的某些化合物在一定条件下可合成CuH,CuH是一种难溶物,它能在氯气中着火,还能与盐酸反应放出气体,请写出这两种反应的化学方程式
▲ , ▲ 。
17.(6分)X、Y、Z是短周期元素的三种常见氧化物。X跟水反应后可生成一种有还原性的不稳定二元酸,该酸化学式是 ▲ ;Y和X的组成元素相同,Y的化学式是 ▲ ;1mol Z加热时跟水反应的产物需要用6mol的氢氧化钠才能完全中和,Z的化学式是 ▲ ,其中和产物的化学式是 ▲ 。在一定条件下,Y可以跟非金属单质A反应生成X和Z,其反应的化学方程式是 ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com