
题目列表(包括答案和解析)
21、(6分)火力发电厂燃烧煤的废气中往往含有有害气体SO2,为了变废为宝,常常用粉未状的碳酸钙或熟石灰的悬浊液洗涤废气,反应产物为石膏,请回答:
(1)写出上述两个的反应的化学方程式:
(2)试说明用熟石灰的悬浊液,而不用澄清石灰水洗涤废气的理由 22、(4分)(1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式: (2)在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:
20、将NaCl和NaBr的混和物m克溶于足量的水配成500毫升的溶液A,再向其中通入足量的氯气,充分反应后蒸发至干,得干燥晶体(m-2)克,则A溶液中Na+、Br-、Cl-的物质的量浓度之比不可能为( ) A、3:2:1 B、3:1:2 C、4:3:1 D、3:1:4
福建仙游私立一中高考总复习
化学单元测试卷(一)
(满分100分,考试时间90分钟) 命题:张明昭
第Ⅰ卷(选择题,共60分)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
|
|
|
|
|
|
|
|
|
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
|
|
|
|
|
|
|
|
|
|
第Ⅱ卷 ( 非选择题,共40分)
19、直接测定同素异形体相互转化的反应热是很困难的。盖斯定律指出:“不管化学过程是一步完成还是分几步完成,其总过程的热效应是相同的”。已知:
P4(固、白磷)+5O2(气) == P4O10(固) ;
△H=-2983.2KJ·mol-1
P(固、红磷)+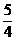 O2(气) ==
O2(气) == 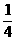 P4O10(固) ;
△H=-738.5KJ·mol-1
那么,1摩白磷转变成相应物质量的红磷时,应是 ( )
A、放出29.2KJ热量 B、吸收29.2KJ热量
C、放出2244.7KJ热量 D、吸收2244.7KJ热量
P4O10(固) ;
△H=-738.5KJ·mol-1
那么,1摩白磷转变成相应物质量的红磷时,应是 ( )
A、放出29.2KJ热量 B、吸收29.2KJ热量
C、放出2244.7KJ热量 D、吸收2244.7KJ热量
18、炽热的炉膛内有反应:C(固)+O2(气)=CO2(气) ; △H=-392KJ·mol-1
往炉膛内通入水蒸气时,有如下反应:
C(固)+H2O(气)=CO(气)+H2(气) ; △H=+131KJ·mol-1
CO(气)+ O2(气)=CO2(气) ; △H=-282KJ·mol-1
O2(气)=CO2(气) ; △H=-282KJ·mol-1
H2(气)+  O2(气)=H2O(气) ; △H=-241KJ·mol-1
O2(气)=H2O(气) ; △H=-241KJ·mol-1
由以上反应推断往炽热的炉膛内通入水蒸气时 ( )
A、不能节省燃料,但能使炉火瞬间更旺 B、虽不能使炉火更旺,但可以节省燃料
C、既能使炉火更旺,又能节省燃料 D、既不能使炉火更旺,又不能节省燃料
17、某温度下,将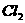 通入
通入 溶液中,反应得到
溶液中,反应得到 的混合液,经测定
的混合液,经测定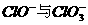 的浓度之比为1:3,则
的浓度之比为1:3,则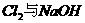 溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为( )
溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为( )
A、21:5 B、11:3 C、3:1 D、4:1
16、有a、b、c、d、e五种物质,它们是硫及其化合物,已知在一定条件下有如下转化关系(未配平):

则这些物质中硫元素的化合价或平均化合价由低到高的顺序是( )
A、a、b、c、d、e B、d、c、a、b、e
C、e、b、a、c、d D、b、a、c、e、d
15、两份铝,一份加入强碱液,一份加入盐酸中,假设酸碱过量,要使前后反应收集到的氢气质量之比为1:2,则两份铝的质量比为 ( )
A、1:2 B、2:1 C、1:4 D、1:1
14、已知下列三个反应:
2Fe2++Cl2 == 2Fe3++2Cl- 2Fe3++Cu == 2Fe2++Cu2+ Fe+Cu2+ == Fe2++Cu
试推断结论:
具有还原性物质的还原性强弱:
①Fe>Cu>Fe2+>Cl- ②Cl->Fe2+>Fe>Cu
具有氧化性物质的氧化性强弱:
③Fe3+>Cl2>Fe2+>Cu2+ ④Cl2>Fe3+>Cu2+>Fe2+ 其中结论正确的是 ( ) A、①③ B、②③ C、①④ D、②④
13、硫代硫酸钠可作为脱氯剂,已知25.0mL 0.100 mol·L-1 Na2S2O3溶液恰好把224mL(标准状况下)Cl2完全转化为Cl-离子,则S2O32-将转化成( )
A、S2- B、S C、SO32- D、SO42-
12、在氧化还原反应3S+6KOH=K2SO3+2K2S+3H2O中,被氧化与被还原的硫原子数之比为( )
A、1 :1 B、2 :1 C、1 :2 D、3 :2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com