
题目列表(包括答案和解析)
21.(8分)含有18个电子的共价化合物中,除HCl、H2S、PH3、SiH4外,另外的符合此条件的4种化合物的化学式为___________、___________、___________、____________。
20.(12分)设计4种不同类的验方法,证明盐酸的酸性强于碳酸。
|
编号 |
实验方法 |
实验现象 |
结论与解释 |
|
1 |
|
|
|
|
2 |
|
|
|
|
3 |
|
|
|
|
4 |
|
|
|
19.(8分)实验室有一瓶混有少量NaCl杂质的N aOH固体试剂。为准确测量其纯度,采用盐酸滴定法进行测定。
①称取WgNaOH固体配成100.00mL水溶液备用;
②将浓度为Cmol/L的标准盐酸装在用标准盐酸润洗过的25.00mL酸式滴定管中,调节液面位置在零刻度线以下,并记下读数为V1mL:
③取V2mLNaOH待测溶液置于洁净的锥形瓶中,加入2-3滴酚酞指示剂后摇匀,然用浓度为Cmol/L的标准盐酸滴定,终点时滴定管的读数为V3mL。
试回答:
(1)配制准确浓度的NaOH溶液,必须使用的主要容器是_______________。
(2)滴定终点时溶液颜色由___________色突变为__________色。
(3)实际用去标准盐酸的体积为___________mL。
(4)若有1mol/L和0.1mol/L两种标准盐酸可供选用,应该使用__________mol/L的盐酸,原因是______________________________________________________________。
(5)若滴定前滴定管尖嘴处有气泡,滴定中气泡被排出,会使碱液的测定值偏_______。
(6)用蒸馏水润洗而不用标准盐酸润洗滴定管,会使碱溶液的测定值偏__________。
18.CuI是一种白色不溶于水的固体,以石墨(阴)和铜(阳)为电极组成电解槽,以含有酚酞和淀粉的KI水溶液为电解液。电解开始后不久,阴极区溶液呈红色,而阳极区仍为无色。过了相当长的时间后,阳极区才呈浅蓝色,则电解开始时电极反应为( )
|
选项 |
阳极反应 |
阴极反应 |
|
A |
Cu-2e=Cu2+ |
Cu2-+2e=Cu |
|
B |
2Cu+2I--2e=2CuI |
2H++2e=H2 |
|
C |
2I--2e=I2 |
2H++2e=H2 |
|
D |
Cu-2e=Cu2+ |
2H++2e=H2 |
17.分别在pH=1的酸溶液和pH=14的NaOH溶液中加入足量的铝,放出H2的量前者多,其原因可能是( )
A.两种溶液体积相同,酸是强酸
B.两种溶液体积相同,酸是弱酸
C.酸溶液的体积比NaOH溶液体积大
D.酸是强酸,且酸溶液的浓度比NaOH溶液浓度大
16.A、B、C、D是四种短周期元素,A元素的最高价氧化物的水化物与它的气态氢化物反应得到离子化合物E,1mol该化合物含有42mol电子;B原子的最外层电子数是次外层电子数的3倍;C元素是植物生长的营养元素之一,原子的最外层电子数是内层电子数的一半;D原子核内没有中子。则( )
A.离子化合物E的化学式为NH4NO3
B.B、D的元素符号分别为氧和氢
C.C元素是氮元素
D.由A、B、C、D四种元素共同组成的盐可超过4种
15.装置如下图所示。药品A、D不溶于水,B、C是液体。甲、乙、丙、丁各装置分别起到制气、除杂、转化、有害尾气处理等作用。若丁处澄清石灰水变浑浊且逸出的气体可点燃,则下列各组中A、B、C、D药品正确的是( )
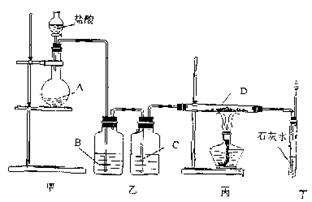
A.CaCO3、饱和NaHCO3溶液、浓H2SO4、C(木炭)
B.锌粒、NaOH溶液、浓H2SO4、Fe2O3
C.MnO2、NaOH溶液、浓H2SO4、Cu
D.Na2SO3、NaOH溶液、浓H2SO4、C(木炭)
14.某种干燥粉末混合物可能由Na2O、Na2CO3、Na2O2、NaCl、NaHCO3中的两种或几种组成(假设固体混合时不反应)。若将春先与足量盐酸反应则逸出气体a,当a缓慢通过足量的NaOH溶液时气体体积缩小(同温、同压),但仍有剩余。另取原混合物在空气中加热至气体汪再发生,发现剩余固体的质量增加,则对原混合的叙述正确的是( )
A.一定含有Na2O和NaCl
B.一定含有Na2O、Na2O2、NaHCO3
C.不含有Na2CO3、Na2O2
D.不含有Na2CO、NaHCO3
13.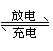 氢镍电池是近年开发出来的可充电电池,它可以取代会产生镉污染的镉镍电池。氢镍电池的总反应式是
氢镍电池是近年开发出来的可充电电池,它可以取代会产生镉污染的镉镍电池。氢镍电池的总反应式是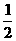 H2+NiO(OH)
Ni(OH)2。根据此反应式判断,下列叙述中正确的是( )
H2+NiO(OH)
Ni(OH)2。根据此反应式判断,下列叙述中正确的是( )
A.电池放电时,电池负极周围溶液的pH不断增大
B.电池放电时,镍元素被氧化
C.电池充电时,氢元素被还原
D.电池放电时,H2是负极
12.在强酸性溶液中可以大量共存的离子组是( )
A.CO32-、SO42-、Na+、AlO2- B.SiO32、Na+、K+、Cl-
C.HCO3-、SO42-、Na+、S2- D.SO42-、Cl-、Na+、NH4+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com