
题目列表(包括答案和解析)
15.(10分)化合物BrFx与水按物质的量之比3:5发生反应,其产物为溴酸、氢氟酸、单质溴和氧气。
(1)BrFx中,x=______________________。
(2)该反应的化学方程式是:______________________________________。
(3)此反应中的氧化剂和还原剂各是什么?______________________________。
14.(8分)填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号:__________________。
(2)周期表中位于第8纵行的铁元素属于第______________族。
(3)周期表中最活泼的非金属元素位于第_________纵行。
(4)所含元素超过18种的周期是第_________、__________周期
13.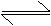 反应L(固)+aG(气)
bR(气)达到平衡时,温度和压强对该反应的影响如下图所示,图中:压强p1>p2,X轴表示温度,Y轴表示平衡混合气中G的体积分数。据此可判断:
反应L(固)+aG(气)
bR(气)达到平衡时,温度和压强对该反应的影响如下图所示,图中:压强p1>p2,X轴表示温度,Y轴表示平衡混合气中G的体积分数。据此可判断:
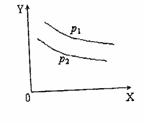 A.上述反应是放热反应
B.上述反应是吸热反应
A.上述反应是放热反应
B.上述反应是吸热反应
C.a>b D.a<b
第II卷(非选择题 共104分)
12.将一定质量的Mg 、Zn、Al混合物与足量稀H2SO4反应,生成H22.8L(标准状况),原混合物的质量可能是( )
A.2g B.4g C.8g D.10g
11.下列反应的离子方程式正确的是( )
A.硫酸铝溶液和小苏打溶液反应 Al3++3HCO3-==3CO2↑+Al(OH)3↓
B.向Ca(ClO)2溶液中通入二氧化硫 Ca2++2ClO-+SO2+H2O==CaSO3↓+2HClO
C.硫化亚铁中加入盐酸 S2-+2H+== H2S↑
D.钠和冷水反应 Na+2H2O==Na++H2↑+2OH-
10.为制备干燥、纯净的CO2,将大理石和盐酸反应生成的气体先后通过装有下列物质的两个吸收装置,两个装置中应依次装入( )
A.水;无水CaCl2 固体 B.饱和NaHCO3溶液,浓H2SO4
C.浓H2SO4;饱和Na2CO3溶液 D.饱和 Na2CO3溶液;稀H2SO4
9.下列各组离子在溶液中既可以大量共存,且加入氨水后也不产生沉淀的是( )
A.Na+ Ba2+ Cl- SO42- B.H+ NH4+ Al3+ SO42-
C.K+ AlO2- NO3- OH- D.H+ Cl- CH3COO- NO3-
8.下列各组混合物不能用分液漏斗分离的是( )
A.硝基苯和水 B.苯和甲苯 C.溴苯和NaOH溶液 D.甘油和水
7.第四周期某主族元素的原子,它的最外电子层上有两个电子,下列关于此元素的叙述正确的是( )
A.原子半径比钾的原子半径大 B.氯化物难溶于水
C.原子半径比镁的原子半径大 D.碳酸盐难溶于水
6.若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是( )
A.生成了一种强酸弱碱盐 B.弱酸溶液和强碱溶液反应
C.强酸溶液和弱碱溶液反应 D.一元强酸溶液和一元强碱溶液反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com