
题目列表(包括答案和解析)
5.下列操作正确的是 (A)金属钠保存在冷水中 (B)在制取乙酸乙酯的实验中,将导管伸进饱和碳酸钠溶液 (C)用适量苯和液溴混合制溴苯时,只需加铁屑,不必加热 (D)用二硫化碳清洗沾有红磷的试管
4.18世纪70年代,瑞典化学家舍勒在研究一种白色、难溶于水的盐时发现,在黑暗中此盐并无气味,而在光照时开始变黑并有刺激性气味的气体产生,此盐是 (A)氟化银 (B)氯化银 (C)溴化银 (D)碘化银
3.下列各种说法中,都包含有前后两个数值,其中前者大于后者的是 (A)铝离子(Al3+)和钠离子(Na+)的半径 (B)16O和18O原子中的中子数 (C)相同温度下,浓度分别为0.1 mol·L-1和0.01 mol·L-1醋酸溶液中CH3COOH的电离度 (D)相同条件下,浓度均为0.l mol·L-1 Na2CO3和NaHCO3溶液的 pH
2.下列各种变化中,不属于化学变化的是 (A)向鸡蛋白溶液中滴入饱和硫酸被溶液,拆出白色沉淀 (B)加热胆矾得到白色的无水硫酸铜粉末 (C)向沸水中滴人饱和氯化铁溶液,制取氢氧化铁胶体 (D)向鸡蛋白溶液中滴人硝酸铅溶液,析出白色沉淀
1.我国某些城市和地区严格禁止生产和销售含磷洗涤剂.含磷洗涤剂主要是添加了三聚 磷酸钠,禁止使用的原因是 (A)三聚磷酸钠会引起白色污染 (B)三聚磷酸钠会跟硬水中的Ca2+、Mg2+形成沉淀堵塞下水管道 (C)三聚磷酸钠会造成自然水质的富营养化,使水生植物大量繁殖,水质变坏 (D)三聚磷酸钠价格昂贵,使用成本高
23、(1)1﹕50,根据勒沙特列原理,过量而廉价的氧气可提高二氧化硫的转化率。(2)废气中每小时排放SO2的体积为1000×5×0.2%=10L,每小时氨气与废气中SO2混合的体积比为2﹕1,恰好与反应中生成(NH4)2SO4的物质的量一致。(3)3.54t硫酸铵,0.91t氨气
23.现有一份“将SO2转化为(NH4)2SO4”的资料,摘录如下:
“一个典型实例:初步处理后的废气含0.2%的二氧化硫和10%的氧气(体积分数)。在400℃时废气以5m3·h-1的速率通过五氧化二钒催化剂层与20L·h-1的速率的氨气混合,再喷水,此时气体温度由400℃降至200℃,在热的结晶装置中得到硫酸铵晶体”(气体均已拆算为标准状况)。
利用上述资料,用氨来除去废气中的二氧化硫,回答下列问题:
(1)按反应中的理论值,二氧化硫和氧气的物质的量之比为2﹕1,该资料中这个比值是______,简述不采用2﹕1的理由__________________
(2)通过计算,说明为什么废气以5m3·h-1速率与20L·h-1的速率氨气混合?
(3)若某厂每天排放1×104m3这种废气,按上述方法该厂每月(按30天)可得硫酸铵多少吨?消耗氨气多少吨?
化学反应速度、化学平衡
1CD、2A、3C、4B、5C、6C、7B、8C、9AC、10C、11D、12A、13B、14CD、15CD、16D、17D、18D、19、AC、20、C;21(1)H++OH-→H2O;平衡向脱矿方向移动。5Ca2++3PO43-+F-→Ca5(PO4)3F、多吃含钙食物。22、(1)增大、增大、(2)否、大于、(3)略;
22、高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g)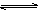 Fe(S)+CO2(g)-Q
其平衡常数可表达为:K==[CO2]/[CO],已知1100℃时K=0.263。
(1)温度升高时,化学平衡移动达到后达到新的平衡,高炉内CO2
和CO的体积比值为------,平衡常数K值______(本大题空格均选:增大、减小或不变)。
(2)1100℃时测得高炉中[CO2 ]=0.025mol/L,[CO]=0.1mol/L,在这种情况下,该反应是否处于平衡状态_______(填是或否),此时,化学反应方程式应速率是V(正)____V(逆)(填大于、小于或等于),其原因是__________________________________________。
Fe(S)+CO2(g)-Q
其平衡常数可表达为:K==[CO2]/[CO],已知1100℃时K=0.263。
(1)温度升高时,化学平衡移动达到后达到新的平衡,高炉内CO2
和CO的体积比值为------,平衡常数K值______(本大题空格均选:增大、减小或不变)。
(2)1100℃时测得高炉中[CO2 ]=0.025mol/L,[CO]=0.1mol/L,在这种情况下,该反应是否处于平衡状态_______(填是或否),此时,化学反应方程式应速率是V(正)____V(逆)(填大于、小于或等于),其原因是__________________________________________。
(MCES-98)三.综合题
21.牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在如下平衡:

进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会腐蚀,其原因是_____________
____________________________________________________________.
已知Ca5(PO4)3F(固体)的溶解度比上面的矿物的溶解度更小,质地更硬,请用离子方程式表示,当牙膏中配有氟化物添加剂后能防止龋的原因是:
_____________________________________________________________________.
根据上述原理,请你提出一种其它捉进矿化的方法:________________________________.
20、已知反应A+3B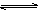 2C+D在某段时间内以A的浓度变化表示的化学反应速率为1 mol·L-1·S-1,则此段时间内以C的浓度变化表示的化学反应速率为( )
2C+D在某段时间内以A的浓度变化表示的化学反应速率为1 mol·L-1·S-1,则此段时间内以C的浓度变化表示的化学反应速率为( )
A.0.5 mol·L-1·S-1 B.1 mol·L-1·S-1 C.2 mol·L-1·S-1 D.3 mol·L-1·S-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com