
题目列表(包括答案和解析)
14.工业废气中氮氧化物是主要的大气污染源之一。
已知2NO2+2NaOH=NaNO3+NaNO2+H2O, NO2+NO+2NaOH=2NaNO2+H2O。
现有a mol NO2和b mol NO的混合气,若用足量的NaOH溶液将其完全吸收,则混合气中两种气体的物质的量必须满足的关系是
A.a=b/3 B.2a=b C.a≥b D.a<b
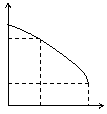
13.将H3PO4溶液逐滴加到60mL的Ba(OH)2溶液中,溶液的pH值与所加H3PO4的体积之间的关系如右图所示(溶液总体积看作两溶液混合后的体积之和),下列说法正确的是
A.c(H3PO4)=0.05mol/L B.pH=7时生成沉淀1.2g
C.pH=a时,生成沉淀0.48g D.pH=a时,溶液中c(OH-)=0.045mol/L
12.10.8g氮的氧化物NxOy 和50g灼热的铁在密闭真空容器中反应一段时间后,生成0.1mol Fe3O4和0.1mol N2,则NxOy是
|
pH
13
a
7
0 20 50 V mL |
 A.NO B. N2O3
C. NO2 D.N2O5
A.NO B. N2O3
C. NO2 D.N2O5
11.液氨溶解碱金属后成为蓝色的导电能力很强的溶液,其颜色被认为是反应生成的电子的氨合物[e(NH3)n]引起的,若放置蓝色逐渐褪去,蒸发褪色后的溶液可以得到白色的氨基钠(NaNH2),反应方程式为:2Na + 2NH3 = 2NaNH2 + H2 ↑ ,据此有关说法不正确的是
A.溶液褪色速率与逸出氢气的速率相对应 B.液氨中有电离过程:2NH3 = NH4+ + NH2-
C.碱金属的液氨溶液是强还原剂 D.液氨是一种非电解质 ,在水中才能电离
10.下列说法正确的是
A.相同温度下,1 mol·L-1氨水溶液与0.5 mol·L-1氨水溶液中,[OH-]之比是2:1
B.在NH3+NaH=NaNH2+H2↑的反应中,NaH为氧化剂
C.0.1 mol·L-1 NH4Cl溶液中的c(NH4+)=c(Cl-)
D.0.2 mol·L-1氨水溶液中,c(NH4+)+c(NH3)+ c(NH3•H2O)= 0.2 mol·L-1
9.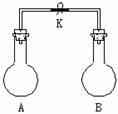 如图所示,室温下,A、B两个容积相等的烧瓶中分别集满了两种气体(同温、同压),当取下K夹,使两烧瓶内气体充分接触后,容器内压强由小到大的顺序正确的是
如图所示,室温下,A、B两个容积相等的烧瓶中分别集满了两种气体(同温、同压),当取下K夹,使两烧瓶内气体充分接触后,容器内压强由小到大的顺序正确的是
|
编 号 |
① |
② |
③ |
④ |
|
A中气体 |
H2S |
H2 |
NH3 |
NO |
|
B中气体 |
SO2 |
Cl2 |
HCl |
O2 |
A. ②③④① B. ③①④② C. ③②①④ D. ④③②①
8.1.92g铜投入一定量浓HNO3中,铜完全溶解,生成气体颜色越来越浅,共收集到672mL气体(标况)。将盛有此气体的容器倒扣在水中,通入标况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积是
A.504mL B.168mL C.336mL D.224mL
7.氮和钠可形成化合物Na3N,它能与水剧烈反应产生NH3,下列叙述正确的是
A.Na3N与水的反应是氧化还原反应 B.Na3N 是共价化合物
C.Na3N若与足量盐酸作用可生成两种盐 D.Na3N中钠离子与氮离子半径相等
6.已知某溶液中存在OH-、H+、NH4和Cl-四种离子,其浓度大小有如下关系:
①c (Cl-)> c (NH4+)> c (H+)> c (OH-) ②c (Cl-)> c (H+)> c (NH4+)> c (OH-)
③c (Cl-)= c (NH4+)且c (OH-)= c (H+) ④c (OH-)> c (H+)> c (Cl-)> c (NH4+)
⑤c (H+)> c (OH-)> c (Cl-)> c (NH4+)。其中可能的是
A.①④ B.③⑤ C.①②③ D.④⑤
5. 往浅绿色的Fe(NO3)2溶液中逐滴加入稀盐酸,溶液的颜色变化应该是
A.颜色变浅 B.变为深绿色 C.没有改变 D.变棕黄色
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com