
题目列表(包括答案和解析)
1.在两个容积相同的容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体。在同温同压下,两容器内的气体一定具有相同的
A.原子数 B.密度 C.质量 D.质子数
18(10分)已知NaCl在60○C时的溶解度为37·1g,现有60○C时的经净化的饱和食盐水685·5g,用“离子交换膜法”将其电解以制取烧碱。电解一段时间后得到密度为1·37g/mL的溶液630g。
(1)电解得到的NaOH主要产生在 区(填“阴极”或“阳极”)。
(2)写出电解NaCl溶液的化学方程式 。
(3)685·5g饱和食盐水中NaCl的质量为 g。
4)电解后溶液中NaCl的物质的量的浓度是多少?
17.(12分)由本题所给①、②两条信息,结合已学过的知识 ,回答下列问题。
①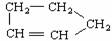 (环戊烯)可简写为
(环戊烯)可简写为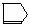 ,其化学性质与烯烃相似。
,其化学性质与烯烃相似。
②烯烃可以与臭氧(O3)反应,再在锌粉存在下水解即可将原有的烯键断裂,断裂处两端的碳原子各结合一个氧原子而生成羰基(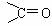 )。这两步反应合在一起,称为“烯键臭氧分解”。如:
)。这两步反应合在一起,称为“烯键臭氧分解”。如:
a.(CH3)2C=CHCH3 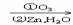 (CH3)2C=O+CH3CHO
(CH3)2C=O+CH3CHO
b. 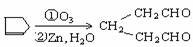
(1)请写出异戊二烯(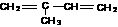 )发生臭氧分解得到的各种产物的结构简式 ,其物质的量之比是 。
)发生臭氧分解得到的各种产物的结构简式 ,其物质的量之比是 。
(2)某有机物A(C6H8)在一定条件下与足量氢气反应可生成饱和有机物B(C6H12),若将A进行“臭氧分解”时,只生成丙二醛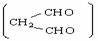 则:
则:
A的结构式为 ,A→B的反应类型为 。
(3)a mol某烃CnH2n-2(分子中无-C≡C-和 ) 结构)发生臭氧分解后,测得有机物中含有羰基bmol,则a和b的代数关系是 或 。H2O
16.(8分)有机物甲、乙的结构简式分别是:
甲:CH3COOCH2CH2OOCCH3
乙:C2H5OOCCOOC2H5
(1)甲和乙的关系是 (填所选选项的代号)。
A.同一物质 B.同分异构体 C.同系物
(2) 通过以下途径可以合成甲、乙(反应条件已略去):
甲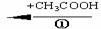 X
X 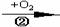 Y
Y 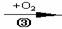 Z
Z 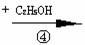 乙+CH3COOH +O2
乙+CH3COOH +O2
试写出:X的结构简式 、反应④的化学方程式
若X与Z在一定条件下可以形成分子式为C4H4O4的酯,则该酯的结构简式为
。
15.(12分)从某盐A的水溶液中出发,有下图所示的一系列变化(参加反应或生成的H2O均末列出)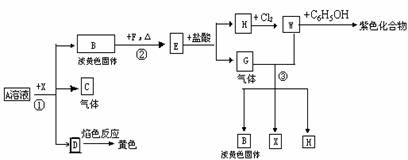
据图回答下列各有关问题:
(1) 写出有关物质的化学式
A ,C ,X 。
(2)反应①的离子方程式是 。
反应②的化学方程式是 。
(3)在反应③中,氧化剂与还原剂的物质的量之比是 。
14.(10分)已知在0.1mol/L的NaHSO3溶液中有关粒子浓度由大到小的顺序是:
c(Na+)﹥c(HSO3-)﹥c(SO32-)﹥c(H2SO3)。
(1)则该溶液中c(H+) c(OH-)(填“﹥”、“﹦”、“﹤”),简述理由
。
(2)现向NaHSO3溶液中,逐渐加入少量含有酚酞的NaOH溶液,可以观察到的现象是 ,写出该反应的离子方程式 。
13. (10分)50mL0.25mol·L-1硫酸与50 mL0.56mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(10分)50mL0.25mol·L-1硫酸与50 mL0.56mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)右图装置与中学教材上实验装置相比较,尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎泡沫塑料的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”、“偏小”、无影响)。
(4)若实验过程中,测得硫酸和NaOH溶液的起始温度的平均值为25.2℃,溶液混合后的最高温度为28.6℃,混合溶液的比热容c (4.18 J/g·℃),硫酸和NaOH溶液的密度都认为是1g·cm-3。则该中和反应的热化学方程式为 。
(5)实验中改用60mL 0.25mol/L硫酸与50mL 0.56mol/L NaOH溶液进行反应,与上述实验相比,所求中和热 (填“相等”或“不相等”)。
(6)若用50mL 0.25mol/L硫酸与50mL0.56mol/L氨水进行上述实验,测得的中和热的数值会 (填“偏大”、“偏小”、“不变”)。
12.Ph=13的强碱溶液和Ph=2的强酸溶液混合,所得混合液的Ph=11,则强碱溶液与强酸溶液的体积比是
A.11︰1 B.9︰1 C.1︰11 D.1︰9
第Ⅱ卷(非选择题 共62分)
11.在一定条件下,将m体积NO和n体积O2同时通入倒立于水中且盛满水的容器内,充分反应后,容器内残留m/2体积的气体,该气体与空气接触后变为红棕色,则m与n的比值是
A..3︰2 B. 2︰3 C. 8︰3 D.3︰8
10.[天河科技3] 在短周期元素X和Y中,X原子的最外层电子数是内层电子总数的一半,Y元素在X的前一周期,Y2-离子和Ne原子的电子层结构相同。关于X和Y形成的化合物Z的说法正确的是
A.Z是一种酸性氧化物 B.Z是一种碱性氧化物
C.Z的分子式一定是X2Y5 D.Z是一种离子化合物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com