
题目列表(包括答案和解析)
1.室温时下列电解质溶液的浓度越大,密度就越小的是 ( )
A.HCl B.HNO3 C.H2SO4 D.NH3·H2O
20.如图所示,x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色
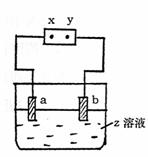 无臭气体放出,下列组合符合这一情况的是
无臭气体放出,下列组合符合这一情况的是
|
19.已知砷(As)是VA族元素,下列对砷及其化合物的叙述中,正确的是
A.砷的原子半径小于磷的原子半径
B.五氯化砷分子中每个原子都满足8电子稳定结构
C.单质砷很容易跟氢气反应生成相应的气态氢化物
D.砷酸的酸性比磷酸的酸性弱
18.已知下列物质在一定条件下氧化KI时,自身发生如下变化:Fe3+→Fe2+;MnO4-→Mn2+;Cl2→Cl-;HNO3→NO。如果分别用等物质的量这些物质氧化足量的KI,得到I2最少的是
A.Fe3+ B.MnO4- C.Cl2 D.HNO3
17.在恒温恒压下,向容积可变的密闭容器中充入3LA和2LB发生如下反应:3A(g)+2B(g) xC(g)+yD(g)达到平衡时,混合气体中D的体积分数为W%,若维持温度、压强不变,将1.2LA, 0.8LB,3LC, 0.6LD作为起始物质充入密闭容器中,达到平衡时混合气体中D的体积分数仍为W%,则x, y的值分别为
xC(g)+yD(g)达到平衡时,混合气体中D的体积分数为W%,若维持温度、压强不变,将1.2LA, 0.8LB,3LC, 0.6LD作为起始物质充入密闭容器中,达到平衡时混合气体中D的体积分数仍为W%,则x, y的值分别为
A.x=3, y=1 B.x=2, y=3 C.x=4, y=1 D.x=5, y=1
16.在下列叙述中能说明盐酸是强酸,醋酸是弱酸的是
A.将pH=4的HCl和CH3COOH稀释成pH=5的溶液,CH3COOH需水量较多
B.HCl和CH3COOH均可用相应的钠盐与浓H2SO4反应制得
C.相同pH值的HCl和CH3COOH溶液中分别加入少量相应的钠盐固体,HCl溶液pH值不变而CH3COOH溶液pH值变大
D.相同pH值的HCl和CH3COOH溶液跟Zn反应,产生H2的起始速率相同
15.将pH等于3的盐酸和pH等于11的氨水等体积混合后,溶液中离子浓度关系正确的是
A.c (NH4+)> c (Cl-)> c (H+)> c (OH-) B.c (NH4+)> c (Cl-)> c (OH-)> c (H+)
C.c (Cl-)> c (NH4+)> c (H+)> c (OH-) D.c (Cl-)> c (NH4+)> c (OH-)>c (H+)
14.下列各选项所述的两个量,前者一定大于后者的是
①F2和Br2的沸点 ②纯水在25℃和80℃时的pH值 ③同温下分别在100g水中最多能溶解的无水CuSO5和CuSO5·5H2O的质量 ④25℃时,等体积的PH值都等于3的盐酸和AlCl3溶液中,已电离的水分子数 ⑤在NH3+NO→N2+H2O反应中,被氧化和被还原的N原子数 ⑥耐火材料MgO和CaO的熔点 ⑦H-和H+离子半径 ⑧金刚石晶体和石墨晶体中,每个最小碳环里所含的实际碳原子数
A.①②⑥⑧ B.①②③⑤ C.②⑥⑦ D.⑤⑥⑦
13.在容积为1 L的固定真空容器中,加入3.68 g N2O4无色晶体,升温至20℃,晶体逐渐气化成无色气体,并部分离解为红棕色的NO2气体,直至达到化学平衡,N2O4(g) 2NO2(g),△H=57 kJ。从化学反应刚发生直到化学平衡的全过程中,以下量变化正确(温度不变)的是
2NO2(g),△H=57 kJ。从化学反应刚发生直到化学平衡的全过程中,以下量变化正确(温度不变)的是
A.气体总压强减少 B.气体的平均相对分子质量减少
C.气体的密度变大 D.气体的密度变小
12.把aL含(NH4)2SO4和NH4NO3的混合液分成两等份,一份用bmol烧碱恰好把NH3全部赶出,另一份与cmol BaCl2使SO42-完全沉淀。则原混合液中NO3-离子的物质的量浓度为
A.(b-2c)/a mol•L-1 B.(2b-4c)/a mol•L-1
C.(2b-c)/a mol•L-1 D.(b-2a)/a mol•L-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com