
题目列表(包括答案和解析)
21.(10分)有人曾建议用AG表示溶液的酸度(acidity grade),AG的定义为
AG=lg([H+]/[OH-])
请回答下列问题:
(1)在25℃时,若溶液呈中性,则AG= 。
(2)在25℃时,若溶液的pH=12,则AG= 。
(3)在25℃时,溶液的pH与AG的换算公式为AG= (要化简)。
(4)在25℃时,将AG=-12的NaOH溶液aL与AG=12的H2SO4溶液bL混合,若所
得混合液的AG=10,则a:b= 。
20.(12分)草酸 在浓H2SO4催化下加热反应的方程式为:
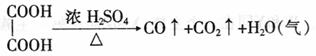
现用图1所示实验装置来检验此反应的所有气体产物,用图2所示实验装置来分离CO和CO2并干燥。图2中a、b分别是玻璃导管和分液漏斗的活塞。

请回答下列问题:
(1)若图1装置中A、B、C三部分仪器的连接顺序改为A、C、B,则可检验出的物质
是 ,不能检验出的物质是 。
(2)图2装置中,分液漏斗所盛的溶液是 ,乙瓶所盛的溶液是 。
(3)简述用图2装置,从开始让混合气体通过甲、乙瓶到收集CO的操作过程:
。
19.(8分)工业制纯碱时,第一步是通过饱和食盐水、氨和CO2反应,获得NaHCO3结晶,它的反应原理可以用下面的方程式表示:
NH3+CO2+H2O===NH4HCO3
NH4HCO3+NaCl(饱和)===NaHCO3+NH4Cl
这两个反应是在一一个反应器中完成的,其总结果是放热反应。
 某研究性学习小组用下列实验装置模拟实现这一过程,并获得NaHCO3结晶。
某研究性学习小组用下列实验装置模拟实现这一过程,并获得NaHCO3结晶。
可选用的实验用品有:①6mol·L-1的盐酸、 ②6mol·L-1的硫酸、③浓氨水
④10%的氢氧化钠溶液、 ⑤澄清石灰水、⑥石灰石 、⑦食盐、⑧蒸馏水 ⑨冰水槽 ⑩其它常用仪器。
请回答下列问题:
(1)写出获得NaHCO3结晶的总反应方程式: 。
(2)A瓶上的分液漏斗内所装的试剂是 (填编号),B瓶内所装的试剂
是 (填编号),C瓶内所装的试剂是 (填编号),A、B、C瓶
中 瓶要放在冰水槽中。

18.在由Fe、FeO和Fe2O3组成的混合物加入100mL1.00mol·L-1的硫酸,恰好使混合物完全溶解,并放出0.448L气体(标准状况),此时溶液中无Fe3+,则下列判断正确的是( )
A.反应后所得溶液中的Fe2+与SO42-的物质的量之比为1:1
B.Fe、FeO、Fe2O3消耗硫酸的物质的量之比为1:1:2
C.混合物里,FeO的物质的量无法确定,但Fe比Fe2O3的物质的量多
D.混合物里,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多
第Ⅱ卷(非选择题 共76分)
17. 两个容积相同的密闭容器A和B中充入SO2和O2,A各为1g,B各为2g,在同温下反应2SO2+O2 2SO3(气)达到平衡。下列说 法中,正确的是 ( )
两个容积相同的密闭容器A和B中充入SO2和O2,A各为1g,B各为2g,在同温下反应2SO2+O2 2SO3(气)达到平衡。下列说 法中,正确的是 ( )
A.平衡时,SO3、SO2、O2在A中的质量分数与在B中的质量分数相等
B.平衡时,SO3、SO2、O2在A中的生成速率与在B中的生成速率相等
C.平衡时,B中气体密度是A中气体密度的2倍
D.平衡时,B中气体压强是A中气体压强的2倍
16.用足量的CO还原48.0g某种氧化物,将生成的气体通入足量澄清石灰水中,得到60.0g沉淀,则该氧化物是 ( )
A.FeO B.Fe2O3 C.CuO D.Cu2O
15.在加热条件下,木炭与浓H2SO4反应,产生的气体所具有的性质是 ( )
A.能使BaCl2溶液变浑浊
B.能使酸性高锰酸钾溶液褪色
C.能使品红试液褪色
D.能使灼热的氧化铜变为亮红色
14.下列离子方程式书写正确的是 ( )
A.少量固体Mg(OH)2溶于饱和NH4Cl溶液中
2NH4++Mg(OH)2===2NH3·H2O+Mg2+
B.氯化铝溶液中加入过量氨水
Al3++4NH3·H2O===AlO2-+4NH4++2H2O
C.烧碱溶液中通入过量二氧化硫
2OH-+SO2===SO32+H2O
D.100mL0.1mol·L-1的NaCO3溶液中加入0.01molCH3COOH
CO32-+CH3COOH===HCO3-+CH3COO-
13.微型银锌电池是电子表和电子计算器的常用电源,其电极分别是Ag2O和Zn,电解质溶液是氢氧化钾溶液,电极反应式分别是 ( )
Zn+2OH--2e====ZnO+H2O Ag2O+H2O+2e====2Ag+2OH-
由此判断,下列说法中错误的是
A.锌是负极,氧化银是正极
B.在外电路中电流由氧化银流向锌极
C.原电池工作过程中,电解质溶液的pH减小
D.原电池反应的总化学方程式是Ag2O+Zn====2Ag+ZnO
12.关于晶本的下列说法中,正确的是 ( )
A.在晶体中只要有阳离子就一定有阴离子
B.离子晶体都是离子化合物
C.分子晶体都是共价化合物
D.原子晶体都是固态单质
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com