
题目列表(包括答案和解析)
9、盛有氯化钡稀溶液的甲乙两试管分别通入SO2至饱和,若向甲试管中加入足量硝酸,乙试管中加入足量氢氧化钠溶液,则下列叙述正确的是
A 甲、乙两试管都有白色沉淀生成 B 甲、乙两试管都没有白色沉淀生成
C 甲试管没有白色沉淀生成而乙试管有 D 甲试管有白色沉淀生成而乙试管没有
8、有一种碘和氧的化合物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式是
A I2O4 B I3O5 C I4O7 D I4O9
7、向稀硫酸中加入铜粉不发生反应。若再加入某种盐,则铜粉可以逐渐溶解。符合此条件的盐是
A NaNO3 B KCl C ZnSO4 D Fe2(SO4)3
6、膦(PH3)又称为磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含之。它的分子是三角锥形。以下关于PH3的叙述正确的是
A PH3是非极性分子 B PH3分子中有未成键的电子对
C PH3是一个强氧化剂 D PH3分子中的P-H键是非极性键
5、可以判断某酸是强电解质的现象是
A 该酸加热至沸腾也不分解 B 该酸可溶解氧化铜
C 该酸可跟石灰石反应,放出CO2 D 该酸浓度为0.01mol·L-1时的pH值为2
4、下列叙述正确的是
A 元素的单质可由氧化或还原含该元素的化合物来制得
B 得电子越多的氧化剂,其氧化性就越强
C 阳离子只能得到电子被还原,只能作氧化剂
D 含有最高价元素的化合物不一定具有强的氧化性
3、下列有关硼元素的叙述中,正确的是
A 从硼的相对原子量为10.8,可判断硼原子核内的中子数为6
B 在三氯化硼分子中,硼原子最外层满足了8电子结构
C 硼元素可以和氢元素结合成为氢化物
D 硼元素与氢氧根结合的化合物是一种强碱
2、将如下卤化物跟浓H2SO4放在烧瓶中共热,可以得到纯净卤化氢气体的是
A NaF B NaCl C NaBr D NaI
1、分别将下列各组物质等体积混合,在室温下激烈振荡,静置后,能够形成均匀溶液的是
A 四氯化碳、碘水 B 甲醇、水 C 甘油、水 D 乙酸乙酯、水
(二)若a、b、c三种元素形成的单质(仍用a、b、c表示)和组成的化合物间反应关系式如下(未配平):
①b+c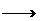 Y
②a+c
Y
②a+c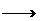 Z
Z
③X+Y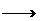 m ④X+Z
m ④X+Z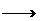 c+n
c+n
⑤Y+Z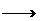 c+n
c+n
回答下列各题:
(1)最有充分理由说明上述反应中一定属于氧化还原反应的是 (填序号),其充分理由是 。
(2)如果m是一种无色、粘稠的油状液体化合物,则Y、Z分别是 ;写出下列反应方程式③ 。
27、(1)某温度下,向某容积固定的密闭容器中加入1molN2和3molH2,使之反应合成NH3,平衡后测得NH3的体积分数为m。若保持温度不变,只改变起始加入量,使之反应平衡后NH3的体积分数仍为m,令X、Y、Z分别代表初始加入的N2、H2、NH3的物质的量。请填写下列空白:
①若X=0,Y=0,则Z= 。
②若X=0.75,Y= ,Z=- 。
③X、Y、Z应满足的一般条件是 。(请用两个方程式表示,其中一个只含X和Z,另一个只含Y和Z)
(2)若维持温度和压强不变,在一个可变容积的容器中发生上述反应。请填写下列空白:
①若X=0、Y=0,则Z= 。
②若X=0.75,则Y= ,Z= 。
③X、Y、Z应满足的一般条件是
28、已知连接羟基的碳原子上没有氢原子的醇不能发生催化氧化反应。A是一种重要的化工原料,其分子组成为C4H9Cl,A有如下转化关系:
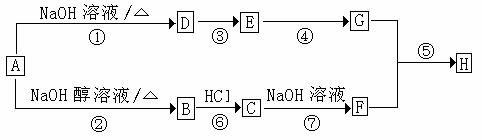
其中F不能发生催化氧化反应,E和G都能和新制Cu(OH)2反应,但反应条件、实验现象不同,H是一种果香味的液体。回答下列问题;
(1)A的同分异构体共有 种,符合条件的A的结构简式为
(2)与①、⑦反应类型相同的反应是 (填序号),若A中混有C,对生成B的纯度是否有影响 (填“是”或“否”),理由是
(3)写出下列反应的化学方程式:
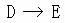
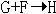
29、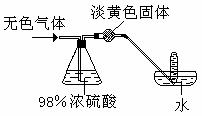 有一无色气体(可能由O2、N2、CO2、HCl、NH3、H2、NO、NO2中的一种或几种组成),如图示通过洗气瓶,发现气体体积减小一部分;通过干燥管后气体呈红棕色,再将该气体适量地通入盛满水倒立于水槽中的试管内,发现试管内水位下降后又缓慢上升,最后试管内全部充满液体。由此判断:
有一无色气体(可能由O2、N2、CO2、HCl、NH3、H2、NO、NO2中的一种或几种组成),如图示通过洗气瓶,发现气体体积减小一部分;通过干燥管后气体呈红棕色,再将该气体适量地通入盛满水倒立于水槽中的试管内,发现试管内水位下降后又缓慢上升,最后试管内全部充满液体。由此判断:
原气体中一定有 、一定没有 。
30、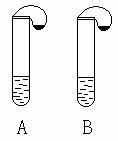 右图所示的A、B两支大试管中各盛有等质量的同一种液体,试管口各系有一个小气球,气球内分别装有等质量的不同固体(纯净物),实验时将两气球抬起,将其中固体同时倾入试管内,固体全部溶解,同时看到两气球都鼓气胀大,但A试管气球胀大的速度及最终胀大的体积都明显大于B。若两试管产生同一种气体,试推测A、B中盛放的液体和固体的可能组合,将各组合填入下表,要求各组分产生的气体不能相同。(可以不填满)
右图所示的A、B两支大试管中各盛有等质量的同一种液体,试管口各系有一个小气球,气球内分别装有等质量的不同固体(纯净物),实验时将两气球抬起,将其中固体同时倾入试管内,固体全部溶解,同时看到两气球都鼓气胀大,但A试管气球胀大的速度及最终胀大的体积都明显大于B。若两试管产生同一种气体,试推测A、B中盛放的液体和固体的可能组合,将各组合填入下表,要求各组分产生的气体不能相同。(可以不填满)
|
组合编号 |
A、B中的液体 |
A中的固体 |
B中的固体 |
产生的气体 |
|
① |
|
|
|
|
|
② |
|
|
|
|
|
③ |
|
|
|
|
|
④ |
|
|
|
|
|
⑤ |
|
|
|
|
|
⑥ |
|
|
|
|
31、50ml 0.5mol·L-1的盐酸与50ml0.55mol·L-1的NaOH 溶液在下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题:
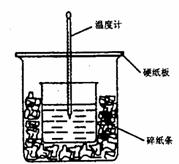
(l)从实验装置上看,图中尚缺少的一种玻璃用品是 。由图可知该装置有不妥之处,应如何改正? 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”“偏小”“无影响”)。
(4)实验中改用 60 mL 0.50 mol· L-1的盐酸跟 50mL 0.55 mol· L-1的 NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”)。简述理由 。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值会 ;用50mL 0.50 mol·L-1的 NaOH溶液进行上述实验,测得的中和热的数值会_(均填“偏大”“偏小”“无影响”)。
32、在下图中,当容器A中的反应开始后,再进行下列操作:
(1)若弹簧止水夹c打开, B容器中有什么现象发生
.
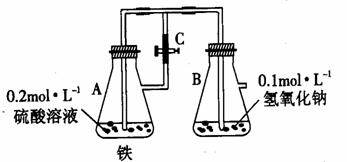 (2)若止水夹C关闭一段时间后,而容器A中的反应仍在进行时,B中有什么现象发生
(2)若止水夹C关闭一段时间后,而容器A中的反应仍在进行时,B中有什么现象发生
,写出B中有关反应的化学方程式 .
(3)若先打开止水夹 C一段时间,让 A中的反应进行,然后再关闭止水夹 C一会儿,B 中所发生的现象是 。其原因是 .
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com