
题目列表(包括答案和解析)
3.去年“非典”在我国广东流行,民间都用过氧乙酸(CH3COOOH)作为消毒剂,因它具有很强的氧化性和腐蚀性,可以迅速杀灭多种微生物,包括多种病毒(如:SARS病毒)、细菌、真菌及芽孢,有关过氧乙酸的叙述不正确的是
A.过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体
B.过氧乙酸与苯酚混合使用杀菌能力更强
C.过氧乙酸因具有强氧化性,所以有杀菌作用
D.在使用过氧乙酸消毒时并不是浓度越大越好
2.在下列各说法中,正确的是( )。
A.△H > 0 kJ·mol-1表示放热反应,△H < 0 kJ·mol-1表示吸热反应
B.热化学方程式中的化学计量数表示物质的量,可以是分数
C.1 mol H2SO4与1 molBa(OH)2反应生成BaSO4沉淀时放出的热叫做中和热
D.1 mol H2与0.5 molO2反应放出的热就是H2的燃烧热
1.某物质的溶液既能使蓝色石蕊试液变红,也能与碳酸盐反应生成气体,此物质有可能是
①氧化物 ②盐 ③碱 ④单质 ⑤酸
A.①②④ B . ①②④⑤
C.② D . ①②③④⑤
13.(16分)由实验得知,用电解法将电解液中的金属离子还原为金属单质时,电极所通过的电量Q正比于金属的物质的量n和金属离子的化合价a的乘积,其比例系数F是一恒量称为法拉第常数。它与金属的种类无关。已知:
阿伏加德罗常数:NA= 6.02×1023mol-1 电子电量:e = 1.6×10-19C M(Cu) = 64g · mol-1
①试求法拉第常数F(电量以库为单位,保留三位有效数字)
②如果电解CuSO4溶液获得1kg的金属铜,通过电解槽的电量是多少?
12.(16分)用实验确定某酸HA是弱电解质。两位同学的方案是:
甲:①称取一定质量的HA配制0.1mol / L的溶液100mL;②用PH试纸测出该溶液的PH值,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制PH=1的两种酸溶液各100mL;②分别取这两种溶液各10mL,加水稀释至100mL;③各取相同体积的两种稀释液装入两个试管,同时加入相同纯度的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第一步中,都要用到的定量仪器是 。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的PH 1(选填>、<、=)。乙方案中,说明HA是弱电解质的现象是 (选填标号,多选扣分):(A)装HCl的试管中放出气体的速率快;(B)装HA溶液的试管中放出气体的速率快;(C)两个试管里产生气体的速率一样快。
(3)请你评价,乙方案中难以做到之处:
难以做到; 难以做到。
(4)请你再提出一个合理而最容易进行的方案(药品可任取),作简明扼要表述。 。
11.(14分)将2mol H2O和2mol CO置于1 L容器中,在一定条件下,加热至高温,发生如下可逆反应:2H2O(g) 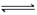 2H2 +O2
2H2 +O2
2CO + O2 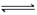 2CO2
2CO2
(1)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是________和________,或________和 ________。(填它们的分子式)
(2)若平衡时O2和CO2的物质的量分别为n(O2)平 = a mol,n(C02)平 = b mol。 试求n(H2O)平 = ________________。(用含a、b的代数式表示)
10.(20分)致冷剂是一种易被压缩、液化的气体,液化后在管内循环,蒸发时吸收热量,使环境温度降低,达到致冷目的。人们曾采用过乙醚、NH3、CH3Cl等作致冷剂,但它们不是有毒,就是易燃、于是科学家根据元素性质的递变规律来开发新的致冷剂。
据现有知识,某些元素化合物的易燃性、毒性变化趋势如下:
(1)氢化物的易燃性:第二周期: > >H2O、HF;
第三周期: SiH4>PH3> > 。
(2)化合物的毒性:PH3>NH3 H2S H2O;
CS2 CO2 CCl4 > CF4 (选填>或<、=)。
于是科学家们开始把注意力集中在含F、Cl的化合物上。
(3)已知CCl4的沸点为76.8℃,CF4的沸点为-128℃,新致冷剂的沸点范围应介于其间。经过较长时间反复试验,一种新的致冷剂氟里昂CF2Cl2终于诞生了,其它类似的还可以是 。
(4)然而,这种致冷剂造成了当今的某一环境问题是 。
但求助于周期表中元素及其化合物的 变化趋势来开发致冷剂的科学思维方法是值得借鉴的。(填写字母,多选扣分)
①毒性 ②沸点 ③易燃性 ④水溶性 ⑤颜色
(a)①②③ (b)②④⑤ (c)②③④
9.从下列实验事实所引出的相应结论正确的是
|
选项 |
实验事实 |
结论 |
|
A |
盐酸中加入相同温度的氨水,反应混合液的温度上升 |
盐类水解过程是吸热的 |
|
B |
在化学反应前后,催化剂的质量和化学性质都没有改变 |
催化剂一定不参与化学反应 |
|
C |
在常温下N2很难与金属化合 |
氮元素的非金属性很弱 |
|
D |
钢比铝容易锈蚀 |
钢中的铁不如铝活泼 |
高三化学复习检测
基本理论
班学生 得分
第Ⅰ卷答案表
第Ⅱ卷(非选择题 共66分)
8.下列事实不能用勒沙特列原理解释的是
A 开启啤酒瓶后,瓶中马上泛起白色泡沫
B 实验室常用排饱和食盐水的方法收集氯气
C 工业上生产硫酸的过程中使用过量的空气以提高SO2的利用率
D 合成氨工业使用500℃的高温以提高单位时间的产量
7.下列叙述正确的是
A 干冰汽化时碳氧键发生断裂
B CaO和SiO2晶体中都不存在单个小分子
C Na2O和Na2O2所含的化学键类型完全相同
D 溴蒸汽被木炭吸附时共价键被破坏
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com