
题目列表(包括答案和解析)
21.(7分)有mA(g)+nB(g) 3C(g)平衡体系,在不同条件下,反应混合物中A、B、C的体积分数和时间t的关系如图4所示:
3C(g)平衡体系,在不同条件下,反应混合物中A、B、C的体积分数和时间t的关系如图4所示:

图4
(1)若图A的a和b两条曲线分别表示有无催化剂的情形,曲线 表示有催化剂的情形。
(2)若图B中c、d两条曲线分别表示不同温度的情形,则曲线 表示高温时的情形。
(3)若图C中e、f表示不同压强时的情形,则曲线 表示压强较大时的情形,方程式中A、B两种物质的系数m、n分别为 、 。
20.(10分)有一学生在实验室测某溶液的pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作是 (填“正确的”或“错误的”),其理由是 。
(2)如不正确请说明理由,同时请分析是否一定有误差?答 。
(3)若用此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 ,原因是 。
19.(5分)利用图3所示装置比较不同电解质在水溶液里电离能力的大小。
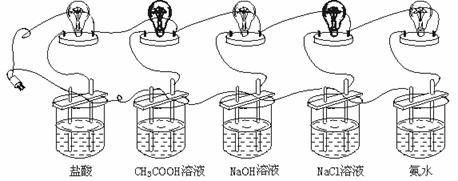
图3
请回答有关问题:
(1)下列不会影响电解质在溶液中电离程度的因素有 。
A.电解质的成键类型
B.电解质本身的颜色
C.溶解电解质所用溶剂的种类
D.电解质溶液的温度
E.电解质溶液的浓度
F.电解质在通常情况下的存在状态
G.外界环境的压强
(2)为了探究不同电解质之间电离能力的差异,课本上设计了上述实验,通过观察灯泡的明亮程度,判断电解质的电离能力大小,为此必须控制其他能影响灯泡亮度的一些因素,使之保持一致,从而不影响灯泡的明亮程度。在本实验中,采取了哪些主要措施来控制其他因素对灯泡亮度的影响?(写出三条即可)
18.同时对农作物施用含氮、磷、钾的三种化肥,对给定的下列化肥:①K2CO3,②KCl,③Ca(H2PO4)2,④(NH4)2SO4,⑤氨水。最适当的组合是
A.①③④ B.②③④
C.①②⑤ D.②③⑤
全国统一标准测试
化 学
第Ⅱ卷
(非选择题 共7题 共55分)
17.在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气。下列说法正确的是
A.甲烧杯中放入锌的质量比乙烧杯中放入锌粒的质量小
B.甲烧杯中的酸过量
C.两烧杯中参加反应的锌的质量相等
D.反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+)小
16.关节炎病因是在关节滑液中形成尿酸钠晶体,尤其在寒冷季节易诱发关节疼痛,其化学机理为:
①HUr+H2O Ur-+H3O+
Ur-+H3O+
尿酸 尿酸根离子
②Ur-(aq)+Na+(aq) NaUr(s)
NaUr(s)
下列对反应②的叙述中正确的是
A.反应的ΔH>0 B.升高温度平衡向正反应方向移动
C.反应的ΔH<0 D.降低温度平衡向逆反应方向移动
15.常温下,向0.1 mol·L?-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图2所示,a、b、c、d分别表示实验时不同阶段的溶液,下列有关说法中不正确的是

图2
A.溶液的pH:a<b<c<d B.溶液的导电能力:a>b>d>c
C.a、b溶液呈酸性 D.c、d溶液呈碱性
14.向10 mL 0.1 mol/L的Na2CO3溶液中通入22.4 mL(标况)CO2,当气体全部溶解时,溶液中粒子浓度关系正确的是
A.c(Na+)>c(CO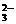 )>c(HCO
)>c(HCO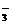 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.c(HCO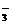 )=c(Na+)>c(OH-)>c(H+)
)=c(Na+)>c(OH-)>c(H+)
C.c(Na+)=c(HCO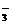 )+c(CO
)+c(CO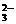 )+c(H2CO3)
)+c(H2CO3)
D.c(OH-)=c(HCO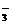 )+2c(H2CO3)+c(H+)
)+2c(H2CO3)+c(H+)
13.在密闭定容容器中有可逆反应:mA(g)+nB(g) pC(g);处于平衡状态,又知,m+n>p,正反应为吸热反应,则下列说法正确的是
pC(g);处于平衡状态,又知,m+n>p,正反应为吸热反应,则下列说法正确的是
①升高温度c(B)/c(C)的比值减小 ②降温时体系内混合气体平均相对分子质量减小
③加入B,A的转化率变大 ④加入催化剂,气体的总物质的量不变 ⑤充入C,则A、B的物质的量增大
A.③④ B.①②⑤ C.②③⑤ D.全部
12.下列反应的离子方程式正确的是
A.FeO与稀HNO3反应:FeO+2H+===Fe2++H2O
B.FeCl3溶液中通入H2S气体:2Fe3++H2S===2Fe2++S↓+2H+
C.NH4Cl固体加入极稀NaOH溶液中:NH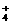 +OH-===NH3↑+H2O
+OH-===NH3↑+H2O
D.氯化铵固体和熟石灰共热
NH +OH-===NH3↑+H2O
+OH-===NH3↑+H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com