
题目列表(包括答案和解析)
3.下列说法正确的是 ( )
A.含非极性键的分子一定是非极性分子,含极性键的分子一定是极性分子
B.在所有晶体中不可能有不含化学键的晶体
C.分子晶体中,分子量小的晶体熔点、沸点不一定比分子量大的低
D.晶体中如果存在金属阳离子,则一定存在阴离子
|
|
|
A.NaCl Na+ :Cl: B.HClO H :Cl:O:
|
|
|
|
C.-CH3 H:C : D.NH4I [H : N :H]+I-
2.将4molA气体和2molB气体在2L的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g)→2C(g),若经2s后达到平衡,测得C的浓度为0.6mol·L-1。现有下列几种说法:①用物质A表示的反应的平均速率为0.3mol/(L·s)②2s时A的转化率为70%③2s时B的浓度为0.7mol/L④平衡时,增加B的量,B的转化率增大,A的转化率下降
其中正确的是 ( )
A.①③ B.②③ C.①④ D.②④
1.“神舟”五号载人飞船发射成功后,我国又在启动“嫦娥工程”,在3-4年内中国人登上月球。人类探测月球发现,其土壤中存在较丰富的质量数为3的氦,它可以作为核聚变的重要原料之一。以下叙述正确的是 ( )
A.由质量数为3的氦原子构成的分子是双原子分子
B.23He与24He的性质均相同
C.23He、24He 形成的分子中存在共价键
D.23He中的质子数与24He的中子数相等
26.A为烃,B为烃的含氧衍生物,由等物质的量的A和B组成的混合物0.05mol在0.125molO2中恰好完全燃烧生成0.1molCO2和0.1mol H2O ,通过计算回答:
(1)从分子组成的角度分析,该混合物的组合可能有几种?
(2)另取一定量的A和B的混合物完全燃烧,将其以任意比混合且物质的量和一定。
①若耗氧一定,则A和B的分子式分别是 、 。
②若生成CO2和H2O的物质的量一定,则A和B的分子式分别是 、 。
25.超细氮化铝粉末被广泛应用于大规模集成电路生产等领域。其制取原理为: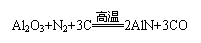
 。由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质。为测定该产品中有关成分的含量,进行了以下两个实验:
。由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质。为测定该产品中有关成分的含量,进行了以下两个实验:
(1)取10.00 g样品,将其加入过量的NaOH浓溶液中共热并蒸干,AlN跟NaOH溶液反应生成NaAlO2,并放出氨气3.36 L(标准状况)。
①上述反应的化学方程式为_______________________________________;
②该样品中AlN的质量分数为_________________。
(2)另取10.00 g样品置于反应器中,通入2.016 L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34 g/L(已折算成标准状况,AlN不与O2反应)。该样品中含杂质炭_______g。
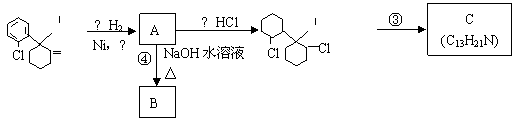
24.“摇头丸”中含有氯胺酮成分。氯胺酮在一定条件下发生下列一系列转化:
 CH3
CH3
CH3
CH3
NH NH·HCl
O
(1)写出氯胺酮的分子式______________________;
(2)上述转化过程中发生取代反应的是____________;
反应③的条件是_____________________。
(3)C的结构简式可能为_________________、___________________。
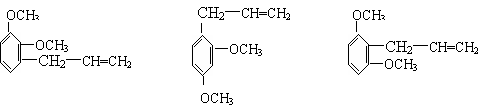
23.(9分)下列三种有机物都是某些植物挥发油中的主要成分。

回答下列问题 ⑴这三种有机物均属于(选填字母)______ a 芳香烃 b 酚类 c 芳香族化合物 d 醛类 ⑵A能发生的反应类型(选填字母)_____ a、消去 b、与氢氧化钠溶液中和 c、加成反应 d、氧化反应 e、加聚反应 f、还原反应 ⑶一定质量的有机物C,在足量的O2中完全燃烧,生成CO2和消耗O2的物质的量之比为_____ ⑷B分子有多种同分异构体,其中均含有两个“-OCH3”和一个“-CH2-CH=CH2”基
团的芳香族化合物有五种,请写出其余两种的结构简式:______________、
______________________
22.已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
① c(Cl-) > c(NH4+) > c(H+) > c(OH-) ② c(Cl-) > c(NH4+) > c(OH-) > c(H+)
③ c(NH4+) > c(Cl-) > c(OH-) > c(H+) ④ c(Cl-) > c(H+) > c(NH4+) > c(OH-)
填写下列空白。
(1)若溶液中只溶解了一种溶质,则该溶质是______________,上述四种离子浓度的大小顺序为________________(填序号)。
(2)若上述关系中③是正确的,则溶液中的溶质为______________________________;
若上述关系中④是正确的,则溶液中的溶质为__________________________________。
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)___________c(NH3·H2O)(填“大于”、“小于”或“等于”,下同),混合前酸中c(H+)和碱中c(OH-)的关系c(H+)____________c(OH-)。
21.(8分)已知A-K所代表的各物质都是中学化学里常见的物质,且I是具有磁性的物质,D和K都具有两性。一定条件下,各物质间的相互反应转化关系如下图所示:
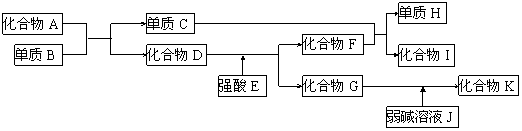
请回答:⑴写出有关物质的化学式:D是_____,H是________。
⑵写出下列反应的化学方程式:
① 化合物G的溶液不呈中性,其原因用离子方程式表示为______________
② C+F→H+I________________________________。
20.实验室里用下图示出的装置制取溴化亚铁。其中,A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈管,e是两只耐高温的瓷夹,其中共盛有56g细铁粉。实验开始时先将铁粉加热至600-700℃,然后将干燥、纯净的CO2气流通入D中,E管中的物质开始反应,不断地将d中的液溴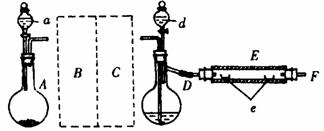 滴入100-120℃的D中,经过几小时的连续反应后在不锈钢管一端沉积有黄绿色鳞片状溴化亚铁80g。
滴入100-120℃的D中,经过几小时的连续反应后在不锈钢管一端沉积有黄绿色鳞片状溴化亚铁80g。
(1)如何检查D装置的气密性?
(2)若导入的CO2不干燥,会在E中发生副反应,其化学方程式为 。
(3)在A中盛有CaCO3,a中盛有6mol·L-1盐酸。为使A中产生的CO2在进入D之前既干燥又纯净,B、C处应设置和各仪器中应盛有何种试剂?
。
(4)实验时,D和E的橡胶塞为什么最好用铝箔包住?
(5)反应过程中要不断地通入CO2,其主要作用是:① ② 。
(6)为防止污染空气,实验时应在F处连接盛有 的尾气吸收装置。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com