
题目列表(包括答案和解析)
1、下列物质中各元素的百分含量总是不变的是( )
A、空气 B、石蜡 C、氨水 D、二氧化氮气体
28.(8分)将固体FeC2O4·2H2O放在一个可以称出质量的容器里加热,固体质量随温度变化的有关典型数据如下表:
|
温度(℃) |
25 |
150 |
300 |
350 |
400 |
450 |
500 |
600 |
650 |
700 |
800 |
900 |
|
固体质量(g) |
1.0000 |
0.9022 |
0.8000 |
0.8000 |
0.4000 |
0.4020 |
0.4444 |
0.4444 |
0.4390 |
0.4300 |
0.4296 |
0.4296 |
据上述数据计算分析
a)300-350℃时质量不变的原因是什么?
b)350-400℃内发生反应的方程式__________________________
c)500℃时固体物质是什么?
d)600-800℃内发生反应的反应式__________________________
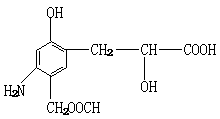
27.(11分)一种含结晶水的羧酸A,在适当条件下完全分解为CO2、CO和H2O,取样6.3克,使其完全分解生成CO2 2.2克、CO 1.4克、H2O 2.7克,若中和0.2520克A需耗去20毫升0.2摩/升 NaOH溶液,若使0.005摩A完全转化为酯,则需要0.46克乙醇,通过计算求:
(1)A的最简式
(2)A的分子式
(3)A的结构简式
26.(15分)某无色溶液,其中有可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO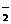 、S2-、CO
、S2-、CO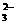 、SO
、SO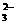 、SO
、SO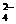 ,现取该溶液进行有关实验,实验结果如下图所示:
,现取该溶液进行有关实验,实验结果如下图所示:

 气体甲 气体乙
气体丙
气体甲 气体乙
气体丙
|
|||
|
|||
|


 无色溶液
溶液甲
溶液乙
溶渡丙
无色溶液
溶液甲
溶液乙
溶渡丙
 浅黄色沉淀甲
白色沉淀乙
白色沉淀丙
浅黄色沉淀甲
白色沉淀乙
白色沉淀丙
试回答下列问题:
(1)沉淀甲是____________,(2)沉淀乙是__________,由溶液甲生成沉淀乙的离子方程式为:_________________________________。(3)沉淀丙是__________。
(4)气体甲成分可能有哪几种?(可以不填满也可以补充,多填要扣分)
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
|
|
|
(5)综合上述信息,可以肯定存在的离子:____________________________________
25.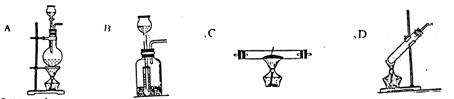 (16分)A-D是中学化学实验中常见的实验发生装置示意图
(16分)A-D是中学化学实验中常见的实验发生装置示意图
(1)请从1-8中选出适当的编号填入A-D的括号中
①亚硫酸钠和浓硫酸反应制取SO2
②过氧化钠和水反应制氧气
③苯和溴反应制溴苯
④无水醋酸钠和碱石灰混和制甲烷
⑤食盐和浓硫酸反应制氯化氢
⑥锌和盐酸反应制H2
⑦铜和氯气反应制无水CuCl2
⑧乙醇和乙酸、浓硫酸混和制乙酸乙酯
A( ) B( ) C( ) D( )
(2)选用装置B做乙炔的发生装置,B中小试管的作用是:__________________。说明能否除去小试管_________________。
23.(8分)以A、B两根石墨棒作电极,电解硝酸银溶液,通电10分钟时,在B极收集到气体11.2毫升(标况)然后将电源反接,以相同的电流强度再通电5分钟,此时与第一次通电前相比较,两极的质量变化分别是A极__________ B极________(填增大、减少、不变) 其数值分别是A_________ B__________ 若溶液的体积为200毫升(设体积不变)则溶液的pH值为___________。
|
①A+NaOH-→D+H2O ②B-→A+H2O ③C+NaOH(适量)-→B+NaCl
④E+H2O-→NaOH+F ⑤C+D+H2O-→B,则A、B、C、D化学式分别是:
A_____________ B_____________ C______________ D_____________
写出4摩C与6摩E在水溶液中发生反应的化学方程式:_______________________
22.(8分)由A、B两气体组成的混合气体8.6克,在标准状况下占有体积为8.96升,已知A和B的物质的量之比为3∶1,摩尔质量之比为14∶1,则A可能为______
_______ ________ B为_________。
21.酸式盐NaHB在水溶液中,HB-的电离程度小于HB-的水解程度,下列说法正确的是
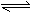 A.HB-水解方程式:HB-+H2O H3O++B2-
A.HB-水解方程式:HB-+H2O H3O++B2-
B.溶液中离子浓度大小为:[Na+]>[HB-]>[OH-]>[H+]
C.NaHB的存在抑制了水的电离
D.相同物质的量浓度溶液的pH值:Na2B>NaHB
第Ⅱ卷(非选择题 共76分)
20.分析有机物的结构应具有的性质是:
①缩聚反应 ②加成反应 ③取代反应 ④水解反应 ⑤中和反应 ⑥显色反应 ⑦氧化反应 ⑧还原反应 ⑨消去反应
A.只③⑤⑥⑦ B.只④⑤⑥⑦
C.全部 D.除①④外其余都有
19.用1kg溶剂中所含溶质的物质的量表示的溶液的浓度叫质量物质的量浓度,其单位是mol/kg。某物质的溶液的质量分数为1.96%,质量物质的量浓度为0.2mol/kg,则该物质可断为
A.NaHCO3 B.CaCO3 C.KHCO3 D.Na2CO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com