
题目列表(包括答案和解析)
8.某溶液中含有Ag+、Ba2+、Mg2+离子,为了将这三种离子逐个进行沉淀分离,加入下列离子的先后顺序正确的是
A.CO32-、Cl-、OH- B.Cl-、OH-、CO32-
C.OH-、Cl-、CO32- D.CO32-、OH-、Cl-
7.近年来,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点。假如硅作为一种普遍使用的新型能源被开发利用,关于其有利因素的下列说法中,你认为不妥当的是
A.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料
B.硅的来源丰富,易于开采,且可再生
C.硅燃烧放出的热量大,且燃烧产物对环境污染程度低,容易有效控制
D.寻找高效催化剂,使SiO2分解产生硅同时释放能量,是硅能源大规模开发利用的一项关键技术
6.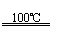
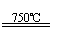 根据“绿色化学”的思想,某化学家设计了下列化学反应步骤:
根据“绿色化学”的思想,某化学家设计了下列化学反应步骤:
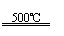
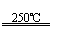 ①CaBr2+H2O CaO+2HBr ②2HBr+Hg HgBr2+H2↑
①CaBr2+H2O CaO+2HBr ②2HBr+Hg HgBr2+H2↑
③HgBr2+CaO HgO+CaBr2 ④2HgO 2Hg+O2↑
该方案的目的是为了制备
A.HBr B.CaO C.H2 D.Hg
5.近年来用红外激光技术研究液氢时,发现分子间作用力也可引起粒子间的反应。在液氢
中有氢分子和质子形成的H3+离子,其构型是等边三角形;H3+还可进一步形成Hn+。下列
判断正确的是
A.H3+可在液氢中开成H5+、H7+、H9+ B.每个H3+粒子中含有2个质子
C.H3+可在液氢中形成H4+、H5+、H6+ D.H3+可广泛存在于固态、液态和气态氢中
4.2003年2月1日美国哥伦比亚号航天飞机在空中解体失事,有专家分析认为,飞机空中解体的最大可能原因是航天飞机机壳底部的石墨瓦在空中脱落,击中机翼。航天飞机表面覆盖石墨瓦,主要是利用石墨
A.具有导电性、防辐射 B.密度小,减轻机身重量
C.熔点高、化学性质稳定 D.硬度小,有润滑作用
3.下列各组中的物质相互作用,水既不是氧化剂,又不是还原剂,且反应属于氧化-还原
反应的是
A.氟气与水 B.铝与氢氧化钠溶液
C.二氧化氮与水 D.五氧化二磷与冷水
2.下列物质露置于空气中易变质的是
①氯水 ②水玻璃 ③烧碱 ④漂白粉 ⑤绿矾 ⑥亚硫酸钠
A.除⑤外 B.除②③外 C.除②③⑥外 D.全易变质
1.我国“神舟五号”航天飞船成功发射升空,表明我国的载人航天技术已经有了突破性的进展。在运送飞船的某些火箭推进器中盛有液态肼(N2H4)和液态双氧水,它们充分混合反应后的产物之一是
A.氧气 B.氮气 C.氨气 D.氢气
29、化学需氧量(COD)是水体质量的控制项目之一,它是量度水中还原性污染物的重要指标。COD是把用强氧化剂(我国采用K2Cr2O7)处理一定量水样时所消耗的氧化剂的量,并换算成以O2作为氧化剂时,1L水样所消耗O2的质量(mg/L).
现有某废水样品20.00mL,加入10.00mL 0。0400mol/L K2Cr2O7溶液,并加入适量酸和催化剂,加热反应2小时。在指示剂存在下用0.100mo/L 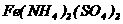 溶液滴定多余的K2Cr2O7,共用去
溶液滴定多余的K2Cr2O7,共用去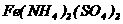 溶液12.00mL。
溶液12.00mL。
(1)已知K2Cr2O7在酸性溶液中作氧化剂时,还原成Cr3+离子,Fe2+离子氧化成Fe3+离子。写出K2Cr2O7与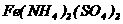 在H2SO4存在下反应的化学方程式。
在H2SO4存在下反应的化学方程式。
(2)计算20.00mL废水所消耗的K2Cr2O7的物质的量。
(3)计算在废水水样的COD
(4)在锻造、机械、印染、造纸、电镀、蓄电池等工厂所排放的污水中,COD特别高的是_________________________。
28、用石墨电极电解500mL0.4mol/L的CuSO4溶液。电解2min放出气体560mL(标况),然后反接再电解4min(假定电流强度和溶液体积不变)
(1)写出反接后的2min电极反应。
(2)电解这6min共放出气体多少mL(标况)?
(3)计算电解后溶液中的氢离子的物质的量浓度。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com