
题目列表(包括答案和解析)
27.(8分)将氮气、氢气按一定比例混合,装入一定容的密闭容器中,在一定条件下进行反应。达平衡时,在反应混合物中,氨气的体积分数为20%。求反应前后(温度相同)容器内气体的压强比。
26. (1)SOCl2+H2O=2HCl+SO2↑ (2)一方面SOCl2因水解而消耗了ZnCl2·3H2O的结晶水;另一方面SOCl2的水解产生的HCl抑制了ZnCl2的水解。
26.(7分)化合物SOCl2常温下为液态,沸点77℃,在盛有10mL水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到反应剧烈,液面上有白雾生成,并有刺激性气味气体逸出,该气体可使湿润品红试纸褪色,轻轻振荡锥形瓶,待白雾消失后,往溶液中滴加AgNO3溶液,有不溶于稀HNO3的白色沉淀生成。
(1)根据上述现象,写出SOCl2与水反应的方程式。
(2)工业上常利用ZnCl2·3H2O和SOCl2混合后共热来制取无水氯化锌,请简述该法的制备原理。
25、(6分)将AlCl3溶液加热,蒸干,灼烧,最后所得到的重要固体产物是什么?用化学方程式加以表示,并配以必要的文字说明。25. Al2O3。AlCl3+3H2O Al(OH)3+3HCl为吸热反应,加热使水解平衡向正方向移动,又有HCl挥发,使AlCl3 完全水解得Al(OH)3,加热Al(OH)3使之分解 2Al(OH)3
Al(OH)3+3HCl为吸热反应,加热使水解平衡向正方向移动,又有HCl挥发,使AlCl3 完全水解得Al(OH)3,加热Al(OH)3使之分解 2Al(OH)3 Al2O3+3H2O
Al2O3+3H2O
24.(1)、(a)、(e)、(h) ①→⑦→⑥→⑾ (2)、(a)、(d)、(i);①→④→⑤→⑿
24.(8分)某学生欲用H2O2催化分解来制取氧气,用浓氨水和生石灰反应来制取氨气。现有下列仪器装置(另有短乳胶管)可供选择:


(1)若制取干燥氧气,应选用的仪器是_________________________,按气流方向连接的顺序是________________________________;
(2)若测定生成O2体积以确定H2O2含量应选用的仪器是____________________,按气流方向连接的顺序是________________________________。
23. B
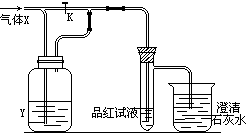
23.(6分)如图是一套检验气体性质的实验装置。向装置中缓慢通入气体X,若关闭活塞K,则品红溶液无变化而澄清的石灰水变浑浊;若打开活塞K,则品红试液褪色。据此判断气体X和洗气瓶内液体可能是( )(用序号填空)
|
序 号 |
A |
B |
C |
D |
|
X |
H2S |
SO2 |
CO2 |
Cl2 |
|
Y |
浓H2SO4 |
NaHCO3饱和溶液 |
Na2SO3溶液 |
NaHSO3饱和溶液 |
22.(10分)环境 监测测定水样中溶解氧的方法是:(A)量取a mL水样,迅速加入固定剂、过量MnSO4溶液和含KOH的KI溶液,密闭摇匀,使之迅速充分地发生反应: 2Mn2+ + O2 +4OH- = 2MnO(OH)2;(B)开瓶塞后即加入适量硫酸使溶液酸化,反应生成I2: MnO(OH)2 +2I- + 4H+ = Mn2++I2+3H2O;(C)用b mol/LNa2S2O3标准液滴定水样中的I2,消耗V mLNa2S2O3:I2+2S2O32-=2I-+S4O62-。
(1) 上述滴定时,待测液中应以_________________为指示剂,以颜色由_______________变______________为滴定终点。
(2) 水样中溶解氧的含量为________________g/L。
(3) a.b两步反应中,____________相当于催化剂。 22 (1)淀粉,蓝,白(或无) (2)8bV/a (3)MnSO4
21.(10分)AB2离子化合物的阴、阳离子的电子层结构相同,化合物AB2中共有54个电子,根据下列反应
(1) AB2 + H2O  X +
H2↑ + B2↑
(2) X + B2 →
Y + AB2 + H2O (3) Y + H2O →
X + Z
X +
H2↑ + B2↑
(2) X + B2 →
Y + AB2 + H2O (3) Y + H2O →
X + Z
推断AB2、X、Y、Z的分子式依次为:AB2__________、X__________、Y__________、Z__________。
写出(1)、(2)、(3)三步反应的化学方程式。
(1)____________________,(2)_________________,
(3)____________________。21. CaCl2 Ca(OH)2 Ca(ClO)2 HClO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com