
题目列表(包括答案和解析)
14.某同学从一种未知的无色溶液中检验出含有Ba2+和Ag+,同时测得溶液的pH=1,他还准备继续检验溶液中是否还含有下列离子:Cl-、S2-、CO32-、SO42-、Cu2+、NO3-、K+、Al3+、NH4+、PO43-,你认为其中不必检验的离子有
A.4种 B.5种 C.6种 D.7种
13.25℃时,硫酸铜的溶解度为sg,把sg无水CuSO4粉末加入到(100+s)g饱和CuSO4溶液中,得到一定量的蓝色晶体,若将此晶体溶解制成饱和溶液,应加入水的质量是
A.100g B.(100+s)g C.(100+9/25)g D.(100-16/25)g
12.下列各项的叙述中都包含两个数值,前一数值大于后一数值的是
A.单质碘中的分子间作用力和干冰中的分子间作用力
B.NaCl晶体中与一个Cl-紧邻的Na+数和CsCl晶体中与一个Cl-紧邻的Cs+数
C.晶体硅中Si-Si键的键能和金刚石中C-C键的键能
D.氨分子中N-H键的键角和甲烷分子中C-H键的键角
11.将3.20g Cu跟10.0mol/L的硝酸30.0mL充分反应,还原产物中有NO和NO2。若 反应后溶液中有a molH+,则此时溶液中NO3-的物质的量为
A.0.5amol B.2a mol C.0.100 a mol D.(a+0.100)mol
10.下列离子在溶液中因发生氧化还原反应而不能大量共存的是
A.K+、Ba2+、OH-、SO42- B.Ag+、NO3-、Cl-、K+
C.H3O+、NO3-、Fe2+、Na+ D.Cu2+、NH4+、Br-、OH-
9.2002年十大科技新闻之一是在世界各地9个研究所39名科学家通力合作下,欧洲核子研究中心成功地制造出约5万个低能量状态的反氢原子。已知反物质的主要特征是电子带正电荷,质子带负电荷。则以下可表示反物质酸与反物质碱进行中和反应实质的离子方程式是
A.H- +OH+====H2O B.H-+OH-====H2O
C.H+ +OH-====H2O D.H++OH+====H2O
8.能够用键能的大小作为主要依据来解释的是
A.常温常压下氯单质与溴单质的状态不同
B.氯化钠的熔点比碘化钠高
C.稀有气体一般难于发生化学反应
D.钠的密度比钾大
7.已知 (钍)原子可发生下列放射性衰变:
(钍)原子可发生下列放射性衰变:
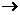
 ,生成的元素与Fr(钫)处于同一周期,以下关于X的推断中错误的是
,生成的元素与Fr(钫)处于同一周期,以下关于X的推断中错误的是
A.X的氢氧化物是一种强碱 B.X的碳酸正盐不溶于水
C.X的原子核外有6个电子层 D.X的最高化合价为+2价
6.以NA表示阿伏加德罗常数,下列说法正确的是
A.0.1molH3O+中含有NA个电子
B.标准状况下,11.2L臭氧中含有NA个氧原子
C.2g重氧水(2H218O)含有NA个中子
D.84gNaHC03晶体中含有NA个CO32-
5.有人认为在元素周期表中,位于ⅠA族的氢元素,也可以放在ⅦA族,下列物质能支持这种观点的是
A.HF B.H3O+ C.NaH D.H2O2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com