
题目列表(包括答案和解析)
22、(9分)某可逆反应为A(气)+B(气) 3C(气),下图中的甲、乙、丙分别表示在不同条件下,生成物C在反应混合物中的体积分数(φ)与反应时间(t)的关系。
3C(气),下图中的甲、乙、丙分别表示在不同条件下,生成物C在反应混合物中的体积分数(φ)与反应时间(t)的关系。
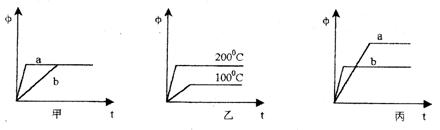
(1)若甲图中的a、b两条曲线分别表示有催化剂和无催化剂的情况,则曲线 表示的是无催化剂时的情况(催化剂一般是指正催化剂)。
(2)若乙图中的两条曲线分别表示在100℃和200℃时的情况,则可逆反应的正反应是
(选填吸热、放热)反应。
(3)若丙图中的a、b两条曲线分别表示在不同压强时的情况 ,则曲线 表示的是压强较大时的情况。
20.(11分)有四支干燥的小试管中,分别装有少量白色物质(约占试管容积的1/10),已知该白色物质肯定是碳酸氢铵、碳酸氢钠、碳酸钠或氯化钠中的一种,现通过加热试管中样品和使用蒸馏水、石蕊试液或pH试纸进行鉴定。
(1)该实验的步骤与内容(略)
(2)请思考并填写下表:
|
白色物质 |
判断依据(现象) |
有关化学方程式(或离子方程式) |
|
碳酸氢铵 |
|
|
|
碳酸氢钠 |
|
|
|
碳酸钠 |
|
|
|
氯化钠 |
|
|
 21(12分)、某同学拟在实验室进行“Na2CO3纯度的分析”实验,
21(12分)、某同学拟在实验室进行“Na2CO3纯度的分析”实验,
下面是他的实验过程:
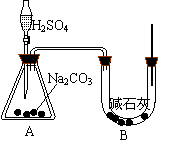
他先设计如右图实验装置,其中A装置盛有无水Na2CO3
试剂(杂质不与水和酸反应)10.0g,分液漏斗内盛有稀硫酸,

 B装置内为碱石灰固体,根据碱石灰质量的增重可计算Na2CO3
B装置内为碱石灰固体,根据碱石灰质量的增重可计算Na2CO3
的纯度。他重复了三次正确操作,结果数据出现了较大偏差。
(1) 你分析出现较大偏差的原因:
。(设原容器内CO2气体的含量可忽略不计,各容器内反应完全。)
通过仔细分析,该同学又设计了一套实验装置(如图),可供选的试剂和药品还有:锌片、浓硫酸、氢氧化钠溶液,碳酸钙固体、蒸馏水。请回答下面问题:
(2)该同学重新设计的装置尚未完整,请在B或D虚框内画出需加上的装置图,并在右下角注明要用到的药品或试剂。
(3)A装置中分液漏斗所盛液体为 。A装置在整套装置中的作用是 。
(4)如果实验后E装置质量增重3.96g,则无水Na2CO3的纯度为 。

19.(8分)把淀粉和NaBr溶液装入半透膜袋,多次浸入蒸馏水中进行分离。请问:
(1)该分离方法称为 。
(2)怎样证明淀粉未透过半透膜而Br-已经透过半透膜?(仪器、试剂任用)
(3)怎样证明淀粉与NaBr已经分离完全?(仪器、试剂任用)
18、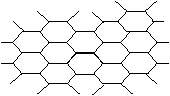 石墨晶体结构如下图所示:
石墨晶体结构如下图所示:
每一层由无数个正六边形构成,
则平均每个正六边所含的碳
原子数为:
A、6 B、4
C、3 D、2
第一学期期中考试
化学试卷
班级 学号 姓名 总分
第Ⅱ卷(非选择题 共78分)
三实验题(本题包括3小题,共31分)
17、在有乙离子存在的情况下,欲用试剂丙来检验溶液中是否含有甲离子,下表所加试剂丙能够对甲离子进行成功检验的是:(说明:在实验过程中不允许加热、过滤、萃取等操作)
|
选项 |
试剂丙 |
甲离子 |
乙离子 |
|
A |
稀盐酸、Ba(NO3)2溶液 |
SO42- |
SO32- |
|
B |
AgNO3溶液 |
Cl- |
I- |
|
C |
KSCN溶液 |
Fe3+ |
Fe2+ |
|
D |
稀氨水 |
Al3+ |
Ag+ |
16.同温同压下,取1 molA和1 molB按A(气)+aB(气) C(气)进行反应,假定平衡时A的转化率为25%,且平衡混和气体的总量变为1.5mol,则a可能是( )
C(气)进行反应,假定平衡时A的转化率为25%,且平衡混和气体的总量变为1.5mol,则a可能是( )
A、a=1 B、a=2 C、a=3 D、a=4
15.已知醋酸的酸性强于苯酚,则相同温度、相同物质的量浓度的四种溶液:①苯酚钠 ②NaHSO4③CH3COONa④NaCl,按pH值由大到小的顺序排列,正确的是( )
A、①>②>③>④ B、④>③>②>① C、①>③>④>② D、③>①>④>②
14.能正确表示下列化学反应的离子方程式是
A 用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32-
B 金属铝溶于盐酸中:Al+2H+=Al3++H2↑
C 硫化钠溶于水中:S2-+2H2O=H2S↑+2OH-
D 碳酸镁溶于硝酸中:CO32-+2H+=H2O+CO2↑
13.某NaOH溶液和0.1mol.L-1的HAc溶液充分混和后,若溶液呈中性,则该混合溶液中有关离子的浓度应满足的关系是( )
A、[ Na+ ]=[ Ac*] B、[ Na+ ]>[ Ac-]
C、[ Na+]<[ Ac-] D、[ Na+]+[ H+]=[ OH-]+[ Ac-]
12.一定条件下,可逆反应C(固)+CO2(气) 2CO(气)+Q(Q>0)达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;
2CO(气)+Q(Q>0)达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;
④减少体系中CO的量;⑤增大反应体系的压强。上述措施中一定能使反应的正反应速率显著加快的是( )
A、①②③④⑤ B、①③④⑤ C、①②⑤ D、①③⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com