
题目列表(包括答案和解析)
25.某天然碱(纯净物)可看作由CO2和NaOH反应后的产物组成。称取天然碱样品四份,溶于水后,分别逐滴加入相同浓度的盐酸30mL,产生CO2的体积(标准状况)如下表:
|
|
Ⅰ |
Ⅱ |
Ⅲ |
Ⅳ |
|
盐酸溶液的体积(mL) |
30 |
30 |
30 |
30 |
|
样品质量(g) |
3.32 |
4.15 |
5.81 |
7.47 |
|
二氧化碳的体积(mL) |
672 |
840 |
896 |
672 |
(1)由第Ⅰ组数据中的CO2体积与样品质量之比,可以推测用2.49g样品进行同样的实验时,产生CO2 mL(标准状况)。
(2)另取3.32g天然碱样品于300℃加热分解至完全(300℃时Na2CO3不分解),产生CO2112mL(标准状况)和水0.45g,计算并确定该天然碱的化学式。
(3)已知Na2CO3和HCl(a g)的反应分下列两步进行:
Na2CO3+HCl→NaCl+NaHCO3
NaHCO3+HCl→NaCl+CO2↑+H2O
由上表中第Ⅳ组数据可以确定所用的HCl(a g)的浓度为 mol·L-1(要有计算过程)。
考试时间:90分钟 命题:高三备课组 校对:严建波 审阅:顾德林 打印排版:顾利吉
第一学期期中考试
24.计算以下两小题时,除必须应用所有给出的数据外,还各缺少一个数据,指出该数据的名称(分别以a和b表示),并列出计算式。
(1)在一定温度和压强下,19.5g A与11.0g B恰好完全反应,生成固体C和3.00L的D气体,计算生成的C的质量(m)。
缺少的数据是:
计算式为:
(2)0.48g金属镁与10mL盐酸反应,计算生成的H2在标准状况下的体积(V)。
缺少的数据是:
计算式为:
23.莫尔盐是硫酸盐的一种复盐,它是一种重要的化学试剂,向它的水溶液中加入KSCN溶液不显红色。莫尔盐的水溶液有如下反应:

根据以上关系,按要求填空:
(1)气体B的分子式为 。
(2)莫尔盐的化学式为 。(不考虑结晶水)
(3)部分沉淀与稀硝酸反应的离子方程式为: 。
22.A是中学化学中常见无机物,A、B、C中含有同一种元素R,不含R的产物已略去,有下图所示主要反应关系:

(1)A与NaOH溶液反应,既可只生成B,也可只生成C,还可以生成B和C。若A为氧化物,则A的化学式(写出两种): 、 。若A为气态氢化物,B中含有A中的两种元素,试写出C与稀H2SO4反应生成A的离子方程式: 。若A为一种铝盐,则B、C的化学式分别为: 、 。
(2)若A的单质与NaOH溶液无论何种物质的量之比反应,产物必为B和C。设R元素在A、B、C中的化合价分别为x、y、z,则x、y、z必须满足的大小关系是(用x、y、z表示): 。
21.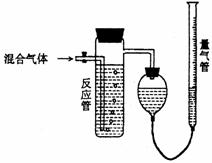 工业上测量SO2、N2、O2混合气体中SO2含量的装置如下图,反应管中装有碘的淀粉溶液,SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O→H2SO4+2HI(不考虑SO2、O2在水中相互反应)
工业上测量SO2、N2、O2混合气体中SO2含量的装置如下图,反应管中装有碘的淀粉溶液,SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O→H2SO4+2HI(不考虑SO2、O2在水中相互反应)
(1)混合气体进入反应管后,量气管内增加的水的体积等于 的体积(填写气体的分子式)。
(2)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量
(选填:偏高,偏低,不受影响)。
(3)反应管内的碘的淀粉溶液也可以用 代替(填写物质名称)。
(4)若碘溶液体积为VamL,浓度为Cmol·L-1,N2与O2的体积为VbmL(已折算为标准状况下的体积)。用C、Va、Vb表示SO2的体积百分含量为 。
(5)将上述装置改为简易实验装置,除导管外,还需选用的仪器为
(选下列仪器的编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶
e.量筒 f.单孔塞 g.双孔塞
20.用下图所示装置(气球内先充有空气)进行铜与稀硝酸反应的实验,请填写下列空格。
(1)实验开始时,先将烧瓶加热,其目的是 。
(2)在不断摇动烧瓶的条件下,使反应充分进行。可观察到4个主要现象:
①铜丝逐渐减少,但不完全消失,且表面有气泡生成;
②气球先略变大,在摇动情况下又变小,
 而后变大;
而后变大;
③ ;
④ ;
(3)摇动情况下,导致气球变小的有关反
应的化学方程式:
, 。
19.在FeCl3和AlCl3混合溶液中先加入过量的NaI溶液,再加入足量的Na2S溶液,则所得的沉淀有 ,写出有关的离子方程式 ,
, , 。
18.0.03mol铜完全溶于硝酸,产生氮的氧化物(NO、NO2、N2O4)混合气体共0.05mol。该混合气体的平均相对分子质量可能是
A.30 B.46 C.50 D.66
17.某溶液中有NH4+、Mg2+、Fe2+和Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是
A.NH4+ B.Mg2+ C.Fe2+ D.Al3+
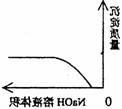
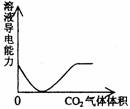
16.下列实验过程中产生的现象与对应的图形相符合的是
A.NaHSO3粉末加入HNO3溶液中 B.H2S气体通入氯水中
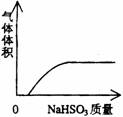
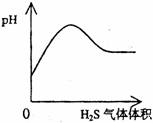
C.NaOH溶液滴入Ba(HCO3)2溶液中 D.CO2气体通入澄清石灰水中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com