
题目列表(包括答案和解析)
4、用石墨电极电解某酸、碱或盐的溶液时,在相同的条件下,阴阳两极收集到的气体的体积比是2∶1,则下列结论正确的是 ( )
A.阴极一定是H2,阳极一定是O2 B.电解后溶液的pH一定变大
C.电解后溶液的pH一定不变 D.电解后溶液的浓度一定变大
3、下列叙述中,正确的是 ( )
A、含有最高价元素的化合物都具有强氧化性
B、阳离子只有氧化性,阴离子只有还原性
C、原子失去电子数越多,还原性越强
D、强氧化剂和强还原剂混合不一定发生氧化还原反应
2、已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是 ( )
A H2O(g)=H2(g)+1/2O2(g); ΔH=+242kJ·mol-1
B 2H2(g)+O2(g)=2H2O(l) ; ΔH=-484kJ·mol-1
C H2(g)+1/2O2(g)=H2O(g); ΔH=+242kJ·mol-1
D 2H2(g)+O2(g)=2H2O(g) ; ΔH=-484kJ·mol-1
1、下列化工生产过程所发生的反应不属于氧化还原反应的是 ( )
A、用油脂制肥皂 B、用铝土矿制金属铝
C、用氯气和消石灰制漂白粉 D、用氢气和氮气合成氨
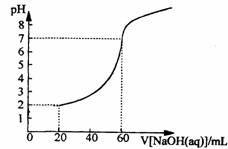
30、20.00mL一定物质的量浓度的盐酸X,用一定浓度的NaOH溶液Y滴定,如图所示。(1)试求X、Y的物质的量浓度之比;(2)求盐酸的物质的量浓度。
29、设计一个实验,能通过观察到的明显的现象,说明CO2与NaOH溶液发生了反应。
实验用品:集气瓶、烧瓶、分液漏斗、长颈漏斗、导管、橡皮管、弹簧夹、烧杯、量筒、水、CO2气体、NaOH溶液以及你认为所能用到的仪器和药品。现有五位同学设计了题29图的五个装置,试回答:

(1)对图A,当将分液漏斗中的NaOH溶液滴入烧瓶时,如果看到水槽中的水被吸入到烧瓶中,则证明CO2与NaOH溶液发生了反应。请写出NaOH溶液与过量CO2反应的离子方程式:
(2)请从图B-E中找出能达到实验目的的装置序号 (用B、C、D、E填空),并将能证明CO2与NaOH溶液发生了反应的操作及实验现象逐一填入下表中:
|
所选的序号 |
操 作 方 法 |
实 验 现 象 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
28、某学生为了测定醋酸溶液中醋酸的含量,进行了如下实验:①准确称取12gNaOH固体,配制1000mL溶液。②取10mL醋酸溶液,用第一步配得的NaOH溶液进行滴定。用去NaOH溶液19.9mL。③重复上述滴定一次,此次用去NaOH溶液20.1mL。
(1)在称样时,若称重前天平的指针偏向于标尺的右方,且把砝码和被称量物质的位置放反;而称量读数时,指针刚好在标尺的零点上。那么所得样品的质量 (填编号:A大于12g;B小于12g;C恰好等于12g;D不能确定。)
(2)配制NaOH溶液所用的主要玻璃仪器中除了玻璃棒、滴管外,还需要 ___________ ;滴定时应选用的指示剂是: 。
(3)终点时,溶液中各离子浓度的大小关系为: 。
(4)由以上数据,计算醋酸溶液中醋酸的质量分数还缺什么物理量: __________ (请注明单位)。如缺少的数据用a表示,则醋酸溶液中醋酸的质量分数为 。
(5)下列操作会使结果偏高的是:( )A、碱式滴定管用蒸馏水洗净后,即注入标准NaOH溶液。B、用酸式滴定管取用待测酸液前,尖嘴部分有气泡,取用过程中气泡消失。
C、滴定前,读碱液体积时仰视;滴定后,读碱液体积时俯视。D、NaOH溶液露置时间太长。
27、将铝件与另一种材料作电极,以某种溶液作电解液进行电解,通电后在铝件与电解液的接触面上逐渐形成一层Al(OH)3薄膜,薄膜的某些部位存在着小孔,电流从小孔通过并产生热量使Al(OH)3分解,从而在铝件表面形成一层较厚的氧化膜。某校研究性学习小组根据上述原理,以铝件和铁棒为电极,一定浓度的NaHCO3溶液为电解液进行实验。
⑴其中铝是此电解池的____极,铁为此电解池的___极(填“阴极”或“阳极”);
⑵铝件表面形成氢氧化铝薄膜的电极反应式为: ;
⑶电解过程中,必须使电解液pH保持相对稳定(不能太大,也不能太小)的原因是
;
⑷使用NaHCO 3溶液为电解液,会减缓阴极区溶液pH的增大,能说明这一原理的离
子方程式为 ;
26、A、B、C是常见的金属化合物的水溶液,M是常见的共价挥发性氢化物,N为M的最高氧化产物的水溶液,将M分别通入A、B、C的反应如下图所示,M与C溶液不发生反应,则:
(1)化学式:A 、B 、M 、N ;
(2)写出下列反应的离子方程式:(Ⅰ) ;
(Ⅱ) ;(Ⅲ) 。
25、纳米材料的表面微粒占总微粒数的比例极大,这是它有许多特殊性质的原因。假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同(如图3所示),则这种纳米颗粒的表面微粒数与总微粒数的比值为:A、7:8;B、13:14;C、25:26;D、26:27。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com