
题目列表(包括答案和解析)
7、实验室用100毫升0.10摩/升盐酸去滴定100毫升0.10摩/升NaOH溶液,如果允许滴定误差为±0.1%,则滴定终点时溶液的pH值范围是
A 5-8 B 3.3-10.7 C 4.3-9.7 D 4.4-10
6、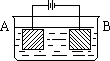 按右图的装置进行电解实验:A极是铜锌合金,B极为纯铜,电解质中含有足量的铜离子。通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68克,溶液质量增加0.03克,则A合金中Cu、Zn原子个数比为:
按右图的装置进行电解实验:A极是铜锌合金,B极为纯铜,电解质中含有足量的铜离子。通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68克,溶液质量增加0.03克,则A合金中Cu、Zn原子个数比为:
A 4︰1 B 3︰1 C 2︰1 D 任意比
4、把a升含(NH4)2SO4和NH4NO3的混和溶液分成两等份,一份加入b mol烧碱并加热,恰好将全部NH4+转变成NH3放出;另一份需含c molBaCl2溶液恰能完全沉淀SO42-,则原溶液中NO3-的物质的的浓度是
A (2b-4c)/a摩/升 B (b-2c)/a摩/升 C (2b-c)/a摩/升 D (b-4c)/a摩/升
3、某氯酸钾样品中含有杂质氯化钾,其中氯元素质量百分含量为a%,则此氯酸钾样品的纯度为
A 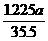 ×100% B
×100% B 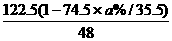 ×100%
×100%
C 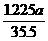 %
D 无法计算
%
D 无法计算
2、在一定温度下,将一包白色的无水硫酸铜粉未投入150克蒸馏水中充分搅拌并过滤,得到一定质量的蓝色晶体和84克滤液,若此温度下无水硫酸铜的溶解度为40克,则这包无水硫酸铜的质量是:
A 66克 B 184克 C 160克 D 90克
12.“二氧化碳是否在有水存在时才能与过氧化钠反应?”这个问题实验室里可通过以下实验 加以说明:
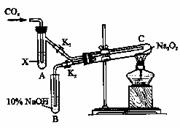
①按图装置,在干燥的试管C中装入Na2O2后,在通入CO2之前,应事先用弹簧夹(K1 、K2)夹持好,其目的为 。
②试管A内的试剂X应是 时,打开弹簧夹K1、K2,加热试管C约几分钟后,将火星的小木条插入试管B的液面上,可观察到带火星的小木条不能剧烈地燃烧起来,且试管C内淡黄色粉末未发生变化。则所得的化学结论是 。
③试管A内试剂为CO2饱和水溶时,其他操作同②,通过 的现象可以证明Na2O2与潮湿的CO2能反应且放出O2。
④CO2和Na2O2反应机理也可用示踪原子分析加以证明。请完成下列反应:Na2O2+ C18O2+H218O-- 。
知识点:Na2O2与CO2的反应机理。
能力点:培养学生知识迁移能力以及动手操作能力。
11.工业上生产Na、Ca、Mg都用电解其熔化的氯化物,但钾却不能用电解KCl熔化物的方法制得,因金属钾易溶于熔化的KCl中而有危险.现在生产钾是用金属钠和熔化的KCl反应制取 .有关数据如下:
熔点(℃) 沸点(℃) 密度(g/cm3)
Na 97.8 883 0.97
K 63.7 774 0.86
NaCl 801 1413 2.165
KCl 770 1500升华 1.984
工业上生产金属钾的化学方程式和条件是:KCl+Na 850℃ NaCl+K

(1)工业上制金属钾主要运用到上表所列的哪些数物理常数
(2)工业制金属钾主要应用什么原理使反应变为现实
知识点:离子反应发生的条件、平衡移动的条件.
能力点:知识迁移能力、综合分析推理能力.
9.碱金属如锂、钠、钾、铷等)溶于汞可形成良好的还原剂“汞齐”,取7g碱金属的汞齐与
水作用得到2.24L氢气(标况),并得1L密度为ρg/cm3的溶液,则溶液中溶质的质量分数可以是( )
A.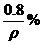 B.
B. 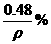 C.
C. 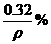 D.
D. 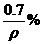
知识点:碱金属、汞的化学性质、质量分数的计算.
能力点:综合分析能力、计算推理能力
8.用洁净的铂丝,蘸取某无色溶液,放在无色火焰上灼烧,透过蓝色钴玻璃观察,火焰呈紫色,下列说法正确的是:( )
A.该溶液只含钾元素的化合物
B.该溶液中一定含钠离子
C.该溶液可能含有钠离子,但一定含有钾离子
D.该溶液可能含有钾离子,但一定含有钠离子
知识点:焰色反应.
能力点:辨别能力、推理能力
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com