
题目列表(包括答案和解析)
25.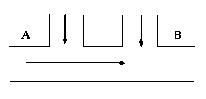 某工厂排出的废水中含氯气,为了除去废水中游离态氯,而且使废水变为中性,有人提出如图所示方案。在废水排出管的A、B处分别注入一定流量的废烧碱溶液和亚硫酸钠溶液。l
某工厂排出的废水中含氯气,为了除去废水中游离态氯,而且使废水变为中性,有人提出如图所示方案。在废水排出管的A、B处分别注入一定流量的废烧碱溶液和亚硫酸钠溶液。l
试写出:(1)A、B处应加入的物质的化学式为______________,_______________。
(2)A、B处反应离子方程式:
A:________________________________________。
B:___________________ _______。
24.从某些方面看,氨和水相当,NH4+和H3O+(常简写为H+)相当,NH2-和OH-相当,NH2-(有时还包括N3-)和O2-相当。
(1)已知在液氨中能发生下列二个反应
NH4Cl+KNH2=KCl+2NH3 2NH4I+PbNH=PhI2+3NH3
请写出能在水溶液中发生的与上二反应相当的反应方程式。
(2)完成并配平下列反应方程式(M为金属):
M+NH3→
MO+NH4Cl→
M(NH2)2→
23.近闻美国和日本正在研究用Na2SO3吸收法作为治理SO2污染的一种新方法,第一步是用Na2SO3吸收SO2;第二步是加热吸收液,使之重新生成Na2SO3,同时得到含高浓度SO2的水蒸汽副产品,试写出上述两步反应的化学方程式
22.A、B两种盐均为无色晶体,其中A的焰色反应呈紫色(透过蓝色钴玻璃),A的水溶液pH大于7。下面是对A、B两种盐所进行的实验记录(见下图),其中H、G均为不溶于酸的白色沉淀。
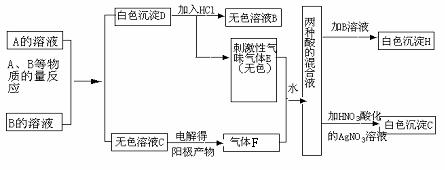
(1)写出A、B两种盐的化学式A ;B 。
(2)写出A、B反应的离子方程式: 。
(3)写出F+E+H2O反应的化学方程式: 。
(4)电解C的无色溶液,阴、阳两极所得气体的体积比理论值为1:1,而实际收集到的气体的体积比却大于1:1,简单解释原因:
21.由于用氯气对饮用水消毒,会使水中的有机物发生氯代,生成有机含氯化合物,与人体有害,世界环保联盟将全面禁止这种消毒方法,建议采用广谱性具有强氧化性的高效消毒剂ClO2。ClO2极易爆炸,生产和使用时尽量用惰性气体稀释,避免光照、震动或加热。
(1)在ClO2分子中,所有原子是否都满足最外层8电子结构? (填“是”或“否”) ,其中氯的化合价是 。
(2)欧洲一些国家用NaClO3氧化浓HCl制ClO2,同时有Cl2生成,且Cl2体积为ClO2的一半,表示这一反应的化学方程式为 。
(3)我国广泛采用将经干燥空气中稀释的氯气通入填有固体亚氯酸钠(NaClO2)的柱内制得ClO2,表示这一反应的化学方程式是 。
我国这一方法较欧洲方法的主要优点是 。
(4)在酸性溶液中,用草酸钠(Na2C2O4)还原NaClO3也可得ClO2,这一反应的离子方程式是 ,此法的优点是 。
20. 某学生拟利用下列两个在室温下能顺利进行的反应,在实验室制取少量纯净的氮气。
某学生拟利用下列两个在室温下能顺利进行的反应,在实验室制取少量纯净的氮气。
3Cl2+2NH3=N2+6HCl NH3·H2O(浓) NH3↑+H2O
实验时,可供选择的仪器装置如下图所示。

实验时可供选择的试剂有:①饱和食盐水,②浓硫酸,③浓硝酸,④浓盐酸,⑤稀烧碱溶液,⑥碱石灰,⑦二氧化锰粉末,⑧浓氨水。
该生设计的实验流程是:

回答下列问题:
⑴在所给出的仪器装置中,要组装成制得纯净的氨的装置,按实验时装置合理连接的先后顺序应依次选取_______(填图中仪器装置的代号);制得纯净的氯气选用的试剂是_________(填试剂的编号)。 ⑵利用浓氨水和氢氧化钠固体制氨时,氢氧化钠固体的作用是__________;此时若用碱石灰代替氢氧化钠,能否达到目的?_____。 ⑶氯气跟氨的反应应在装置__________(填装置代号)中进行,生成的氮气中可能会混有的杂质气体有______________________;若生成的氮气中混有氯气或氯化氢气体,则净化时先后依次通过的试剂是__________(填试剂的编号)。
19.有一瓶澄清的溶液,其中可能含NH4+、K+、Na +、Mg2+、Ba2+、 Al3+、 Fe3+、SO42-、CO32-、NO3- 、Cl-、I-,取该溶液进行如下实验:
⑴用pH试纸检验,表明溶液呈强酸性;
⑵取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置CCl4层呈紫红色;
⑶取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成;
⑷取部分上述呈碱性的溶液,加Na2CO3溶液,有白色沉淀生成;
⑸将⑶得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定并回答:在溶液中肯定存在的上述离子有 ,肯定不存在的上述离子有 ,还不能确定是否存在的上述离子有 。
18.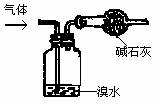 下列四种气体(括号内是混有的少量杂质),其中可用右图所示仪器装置进行净化和干燥的气体是
( )
下列四种气体(括号内是混有的少量杂质),其中可用右图所示仪器装置进行净化和干燥的气体是
( )
A. CO2( HCl) B.C2H6(C2H4)
C.CO2(SO2) D.NH3(N2)
17.下列操作中固体可完全溶解的是 ( )
A. 1mol Al与含1mol H2SO4的稀H2SO4溶液共热
B. 1mol Cu与含2mol H2SO4的浓H2SO4溶液共热
C. 1mol Cu与含4mol HNO3的浓HNO3溶液共热
D.1mol MnO2与含4mol HCl的浓HCl溶液共热
16.氢化铵(NH4H)与氯化铵结构相似,又已知NH4H与水反应有氢气产生,下列叙述不正确的是 ( )
A NH4H的电子式是:
B NH4H固体投入少量水中,有两种气体产生
C NH4H中的H-离子半径比锂离子半径大
D NH4H溶于水后,形成的溶液呈酸性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com