
题目列表(包括答案和解析)
17、不久前,美国加州海军航空站安装了一台250kW的MCFC型燃料电池,该电池可同时供电和蒸汽,其工作温度为600-700℃,所用燃料为氢气,电解质为熔融的K2CO3,已知该电池的总反应为:2H2 + O2 = 2H2O 负极反应式为:H2 + CO32- - 2e- = H2O + CO2,则下列推断正确的是( )
A.正极反应式为:4OH- - 4e- = 2H2O + O2 ↑
B.放电时CO32-向负极方向移动
C.电池供应1mol水蒸气,转移电子为4mol
D.放电时CO32-向负极正向移动
16、根据:S2O82- + 2e- = 2SO42-
Mn2+ + 4H2O = MnO4- + 8H+ + 5e-
推断氧化1.5molMn2+需要S2O82-的物质的量为( )
A.1.5mol B.3.75 mol C.3.25 mol D.3.125 mol
15、膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,存在于电石气的杂质中。它的分子成三角锥形。以下有关PH3的叙述正确的是
A.PH3是非极性分子 B.PH3分子中有未成键电子
C.PH3是一种强氧化剂 D.PH3分子中的P-H键是非极性键
14、同温、同压下同体积的A 、B 两种气体或蒸气的质量比为23:16,当B的分子量为32 时,则A 的分子式不可能是( )
① C2H6O ② CH2O2 ③ 气态烷烃 ④ N2O
A.①、② B.①、③ C.②、③ D.③、④
13、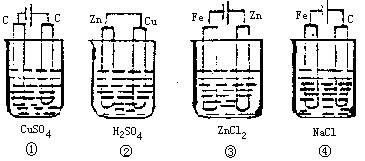 在下边四种装置中,溶液的体积相同,开始时电解质溶液的浓度均为0.10mol· L-1?,工作一段时间后,测得导线上均能通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是:
在下边四种装置中,溶液的体积相同,开始时电解质溶液的浓度均为0.10mol· L-1?,工作一段时间后,测得导线上均能通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是:
A.溶液的pH值:④>③>①>② B.电解质溶液总体积:④=③=②=① C.产生气体总体积:④>③>①>② D.电极上析出的固体质:①>②>③>④
12、下列各溶液中能大量共存的离子组是:
A.使pH试纸呈深红色的溶液中:Fe2+、SO42-、I-、NO3-
B.C(H+)=10-14mol·L-1的溶液中:Na+、AlO2-、S2-、SO32-
C.pH=3的溶液中:Mg2+?、Fe3+?、Cu2+、SO42-
D.使紫色石蕊试液变红色的溶液中:K+、Na+、Ca2+?、HCO3-
11、设NA代表阿伏加德罗常数,下列说法正确的是 A.11.7g食盐晶体中的分子数为0.2NA B.0℃压强为1.01×105帕时,22.4升SO3含分子数为NA
C.常温、常压下,1摩尔甲烷气体含有原子数为5NA D.1摩尔铵根离子所含的质子数为11NA
10、把3摩尔A和2.5摩尔B混合于2升的容器中,发生如下反应:3A(气)+B(气)==2D(气)+XC(气),经5分钟后达到平衡生成1摩尔D,经测定C的平均反应速度为0.1摩/升·分,下列叙述中错误的是( )
A.B的转化率为20%
B.X值是1
C.A的平均反应速度是0.15摩/升·分
D.B的平衡浓度为0.5摩/升
9、根据中学化学教材所附的元素周期表判断,下列叙述不正确的是( )
A.K层电子数为奇数的所有元素所在族的序数与该元素原子的K层电子数相等
B.L层电子数为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C.L层电子数为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等
D.M层电子数为奇数的所有元素所在族的序数与该元素原子的M层电子数相
8、下列离子方程式正确的是( )
A.过量的NaHSO4与Ba(OH)2溶液反应:
Ba2+ + 2OH- + 2H+ + SO42- = BaSO4 ↓+ 2H2O
B.NH4HCO3溶液与足量的氢氧化钠溶液反应:
NH4+ + OH- == NH3↑ + H2O
C.碳酸镁溶于硝酸中:
CO32- + 2H+ = CO2↑ + H2O
D.FeBr2溶液中通入过量氯气:
2Fe2+ + 2Br- + 2Cl2 = 2Fe3+ + Br2 + 4Cl-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com