
题目列表(包括答案和解析)
21.已知A、B分别为两种盐,I为金属单质,J为空气中一主要成分的单质,根据下列框图变化,推断:AgNO3+HCl==AgCl↓+HNO3
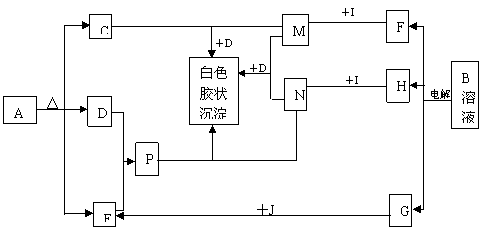
⑴写出下列物质的化学式:A____ B_____ F______ H_____G______
⑵写出C的分子构型_________ D的结构式_____________
E的电子式__________ 分子构型_______________
⑶写出下列反应的离子方程式:
①M+N+D 白色胶状沉淀:__________________________________
白色胶状沉淀:__________________________________
 ②P+N
②P+N 白色胶状沉淀:______________________________________
白色胶状沉淀:______________________________________
20.有A、B、C、D四种单质,在一定条件下,B可以分别和 A、C、D化合生成化合物甲、乙、丙。D和C化合生成化合物丁。已知甲、乙、丙的每个分子中分别含有10个电子,且甲、乙、丙、丁有如下关系:
乙+A=甲+C C+丙 丁+乙 请填写:
⑴单质B的化学式:________________________________
⑵单质A和化合物乙发生反应的化学方程式:__________________________
⑶写出C和D化合生成物质丁的化学方程式:____________________________
⑷根据化合物丙、丁中元素的化合价,判断丙和丁能否在一定条件下发生化学反应生成D,若能写出化学方程式:______________________________。若不能请说出理由:____________________________________________________________________。
19.(6分)在白磷分子中,每个磷原子以________键与另外的_______个磷原子相结合成___________结构,键角为_____。如果把一个白磷分子的每个P-P都打开插入一个氧原子,则一共可结合____个氧原子,这样得到此化合物的分子式为__________。
18.(4分)近闻美国和日本正在研究用Na2SO3吸收法作为治理SO2污染中的一种新的方法:第一步使用Na2SO3的水溶液吸收SO2;第二步是加热吸收液,使之重新生成Na2SO3.同时得到高浓度SO2的水溶液副产品,写出上述两步反应的化学方程式:
①_________________________________________________
②___________________________________________________
17.(4分)化工行业已合成一种硬度比金刚石还大的晶体氮化碳,若已知氮在化合物中显-3价,推断:
⑴其化学式可能是_____________;⑵其晶体类型是_____________;
⑶你认为其硬度比金刚石大的主要原因是________________________________________________________________________________________。
16.下列物质中各原子不是“八电子”稳定结构的是
A.CO2 B.PCl5 C.Na2O D.COCl2
15.下列微粒为正四面体构型的离子是
A.P4(白磷) B.H3O+ C.CH3Cl D.NH4+
14.24mL浓度为0.05mol·L-1的Na2SO3溶液,恰好与20mL浓度为0.02mol·L-1的K2Cr2O7溶液完全反应,则元素Cr在被还原的产物中的化合价是
A.+6 B.+3 C.+2 D.0
13.同周期的三种元素X、Y、Z,已知它们的最高价含氧酸的酸性又强到弱的顺序为HXO4>H2YO4>H3ZO4,则下列叙述不正确的是
A.非金属性X>Y>Z B.X、Y、Z形成阴离子的还原性逐渐增强
C.原子半径X>Y>Z D.X、Y、Z的气态氢化物稳定性由强到弱
12.

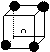
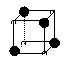 有下列离子晶体的空间结构示意图,以M代表阳离子,以N代表阴离子, 阳离子,·阴离子,化学式为MN3的晶体结构为
有下列离子晶体的空间结构示意图,以M代表阳离子,以N代表阴离子, 阳离子,·阴离子,化学式为MN3的晶体结构为
A B C D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com