
题目列表(包括答案和解析)
3、提纯含有少量硝酸钡杂质的硝酸钾溶液,可以使用的方法为 ( )
A、加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
B、加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
C、加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
D、加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
2、 氯化苄(C6H5CH2Cl)由甲苯和氯反应而合成,反应条件是
(
)
氯化苄(C6H5CH2Cl)由甲苯和氯反应而合成,反应条件是
(
)
A、浓硫酸存在下 B、加热
C、铁粉催化 D、光照
1、要提取食盐中的单质碘,你设计的最佳方法是 ( )
A、萃取 B、重结晶 C、加热 D、过滤
9.现有一定浓度的双氧水溶液、碘化钾溶液、淀粉溶液和蒸馏水等试剂,
请设计一个简单的实验来说明:与一定量的双氧水反应的碘化钾溶液
的浓度越大,反应速率就越快。要求:
(1)写出实验步骤
(2)设计实验表格,用来记录实验步骤和实验现象
7.为证明乙醇分子中含有氧原子,现采用一套装置进行试验,试根据以
下装置示意图、试剂及实验现象,回答有关问题。
Ⅰ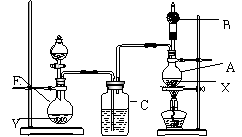 .装置中所装的试剂是:
.装置中所装的试剂是:
①A瓶装无水乙醇,内放无水 盐X
②B干燥管里装生石灰
③C和D中都装浓硫酸
④E瓶中装入试剂Y
Ⅱ.实验操作及现象是:
用水浴加热A瓶,将D中浓硫酸缓缓滴入E中与试剂Y作用;发现C中导管有大量气泡放出;A瓶内X逐渐变色,在B管口挥发的气体可点燃。
请回答下列各问:
⑴E瓶里所装的试剂Y是以下的________;
A.饱和食盐水 B.MnO2和NaCl的混合物 C.浓盐酸
⑵D中浓硫酸所起的作用是_________ ______,C瓶中浓硫酸所起的作用是__ ____________ ;
⑶A瓶中发生反应的化学方程式是______________________________,反应类型是_____________;所生成的___________(写名称)在B出口处点燃;
⑷无水盐X宜选用__________,它能起指示作用的原因是____________;
⑸此实验能验证乙醇分子中含有氧院子的理由是_________________;
⑹如果将装置中的C瓶去掉,实验目的是否能达到___________,因为___________________________________________________________;
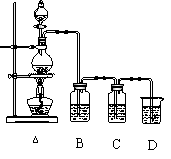
6.实验室可用碳酸钠合成亚硫酸氖晶体。
有关装置如下图所示。将17gNa2CO3溶
于80mL水中,分装在C、D两个锥形瓶
中,再将25g铜屑放入圆底烧瓶中,将
60mL浓H2SO4和10mL水的混合液装在
分液漏斗中,小心加热使SO2逐渐发生。
将SO2通入Na2CO3溶液中至饱和,在合
并C、D两瓶所得的溶液中,慢慢加入17gNa2CO3蒸发浓缩,冷却后得
到亚硫酸钠晶体,回答下列问题:
(1)配制60mL浓H2SO4和10mL水的混合液的操作是_______________;
(2)装置B中H2SO4的作用是___________________________________;
(3)Na2CO3溶液分装在两个锥形瓶中的原因是______________,所发生反应的化学方程式为_____________________________________;
(4)控制SO2产生速度快慢的方法是____________________________;
(5)通入气体结束后,再加入Na2CO3的目的是___________________。
2
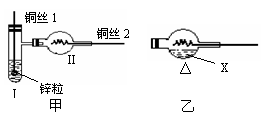
5.如图,用氢气还原氧化铜
的微型快速实验装置。实
验前先将铜丝1的下端弯
曲成一个小圆环,并用铁
锤击成一个带小孔的小匙,
将铜丝2的一端弯曲成螺丝状。
试回答下列问题:
(1)在试管Ⅰ中先加入的试剂是 ;
(2)操作铜丝2的方法是 ;
(3)实验现象是:Ⅰ Ⅱ
(4)这样处理铜丝2的优点是 ,
目的是 ;
 (5)某同学把图甲改成乙,容器内加入某种液体X,稍加热,铜丝操作的方法同铜丝2。若发现铜丝由黑变红,则液体X可能是
。
(5)某同学把图甲改成乙,容器内加入某种液体X,稍加热,铜丝操作的方法同铜丝2。若发现铜丝由黑变红,则液体X可能是
。
4.为了将混有硫酸钠和碳酸氢铵杂质的氯化钠提纯,并得到氯化钠溶液,
有人设计了如下实验:
请回答:
(1)在操作①完成的过程中,盛放药品的仪器名称是 ;
1
(2)操作②中能否选用其它试剂?试简述你的理由。
(3)操作③的目的是 ,
如何判断已达到此目的?
(4)你认为此实验设计是否严密?请说明理由或提出改进方案。
3.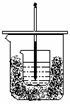 将50mL0.50mol·L-1盐酸与50mL0.55mol·L-1氢氧化钠溶液在下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可以计算出中和热。试回答下列问题:
将50mL0.50mol·L-1盐酸与50mL0.55mol·L-1氢氧化钠溶液在下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可以计算出中和热。试回答下列问题:
(1)从装置上看,尚缺少的一种玻璃用品是 ;
(2)烧杯间填满碎纸条的作用是 ;
(3)大烧杯上如不盖上硬纸板,求得的中和热 (填“偏大”、“偏小”或“无影响”);
(4)若实验中改用60mL0.50mol·L-1盐酸和50mL0.55mol·L-1氢氧化钠溶液进行,与上述实验相比,所放出的热量 (填“相等”或“不相等”);若用浓度和体积都相同的氨水代替氢氧化钠溶液进行实验,测得的中和热数值 (填“偏大”、“偏小”或“无影响”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com