
题目列表(包括答案和解析)
13、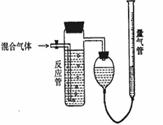 (10分)工业上测定SO2、N2、O2混合气体中SO2含量的装置如下图。反应管中装有碘的淀粉溶液,SO2和I2发生反应为(N2、O2不与I2反应):SO2+I2+2H2O==H2SO4+2HI
(10分)工业上测定SO2、N2、O2混合气体中SO2含量的装置如下图。反应管中装有碘的淀粉溶液,SO2和I2发生反应为(N2、O2不与I2反应):SO2+I2+2H2O==H2SO4+2HI
(1)混合气体进入反应管后,量气管内增加的水的体积等于 的体积(填写混合气体的分子式)
(2)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量 (选填:偏高,偏低,不受影响)
(3)反应管内的碘的淀粉溶液也可以用 代替 (填物质的名称)
(4)若碘溶液体积为Va mL,浓度为Cmol/L。N2与O2的体积为Vb mL(已折算成标准状况下的体积)。用C、Va、Vb表示SO2的体积百分含量为 。
(5)将上述装置改为简易实验装置,除导管外,还需选用的仪器为 。(填写下列仪器似的编号)
a烧杯 b试管 c广口瓶 d容量瓶 e量筒 f单孔塞 g双空塞
14、(14分)SO2是大气污染物之一,为粗略地测定周围环境中SO2的含量,某学生课外活动小组设计了如下实验装置:
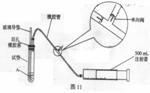
(1)检查该装置的气密性时,先在试管中装入适量的水(保证玻璃导管的下端浸没在水中),然后
(填写操作方法)时,将会看到 (填写实验现象),则证明该装置的气密性良好。
(2)向试管中加入0.0005mol·L-1的碘水1.0mL,用适量的蒸馏水稀释后再加入2-3滴淀粉溶液,配制成溶液A。测定指定地点的空气中SO2的含量时,推拉注射器的活塞反复抽气,A溶液由 色变为 色时反应恰好完全进行,此时停止抽气,该反应的化学方程式为
。
(3)我国环境空气质量标准中对每次空气质量测定中SO2的最高浓度限值如下表:
|
浓度限值/mg·m-3 |
||
|
一级标准 |
二级标准 |
三级标准 |
|
0.15 |
0.50 |
0.70 |
该学生课外活动小组分成第一小组和第二小组,使用相同的实验装置和溶液A,在同一地点、同时测量空气中SO2的含量。当反应恰好完全进行,记录抽气次数如下(假设每次抽气500mL)。请将下表填写完整(计算时保留2倍有效数字):
|
分组 |
第一小组 |
第二小组 |
|
抽气次数 |
120 |
140 |
|
SO2含量/mg·m-3 |
|
|
判断该地点的空气中SO2的含量属于 (填数字)级标准, (“第一”或“第二”)小组的测定结果正确,另一小组实验结果产生较大偏差的原因是(两个小组所用装置和药品均无问题)
。
12、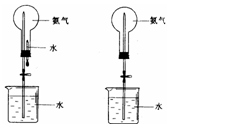 (15分)制取氨气并完成喷泉实验(图中夹持装置均已略去)。
(15分)制取氨气并完成喷泉实验(图中夹持装置均已略去)。
(1)写出实验室制取氨气前化学方程式: ;收集氨气应使用 法,要得到干燥的氨气可选用 做干燥剂。
(2)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷泉的操作是
。该实验的原理是
。
(3)某同学用氨气做喷泉实验时,喷入烧瓶内的水不足烧瓶容积的三分之一,其原因可能是( )
① 瓶塞漏气 ② 用胶头滴管挤入的水太少
③ 喷水用的导管太长 ④烧瓶内未集满氨气,尚有大量空气
A、①②④ B、①③④ C、②③ D、①②③④
(4)在体积为1L的干燥烧瓶中,用排空气法收集氨气后,测得烧瓶中气体的密度是氧气的0.625倍。以此气体进行喷泉实验,当喷泉停止后,进入烧杯中水的体积是( )
A、1/4L B、1/2L C、3/4L D、1L
(5)如果只提供如图2的装置,请说明引发喷泉的方法
。
11、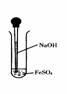 (14分)实验室用如图所示方法制Fe(OH)2,但一般看不到白色沉淀,而是灰绿色转为红褐色的沉淀,请回答:
(14分)实验室用如图所示方法制Fe(OH)2,但一般看不到白色沉淀,而是灰绿色转为红褐色的沉淀,请回答:
(1)滴管下端插入液面的原因是________
_ ;生成红褐色沉淀的化学方程式为______
_ ;此反应中的02可能来自于___________
。
(2)用下面两种方法可以制得白色的Fe(OH)2沉淀。
方法一:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
①用硫酸亚铁晶体配制上述FeSO4溶液时还需加入 。
②除去蒸馏水中溶解的O2常采用 的方法。
③生成白色Fe(OH)2 沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是
。
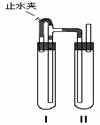 方法二:在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。
方法二:在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。
①在试管I里加入的试是 。
②在试管II里加入的试是 。
③为了制得白色Fe(OH)2沉淀,在试管I和II中加入试剂,打开止水夹,塞子后的实验步骤是
。
④这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是
。
10、(10分)某工厂废液经测定得知含有乙醇、甲醇、乙酸和乙酸乙酯。现欲从废液中回收甲醇、乙醇和乙酸,根据各物质的性质 (见下表) ,补充下列实验步骤,并回答有关问题:
|
物质 |
甲醇 |
乙酸乙酯 |
乙醇 |
乙酸 |
|
沸点/℃ |
65 |
77 |
78 |
118 |
可供选择的实验用品:250 mL 蒸馏烧瓶,400 mL 烧杯,250 mL 烧杯,温度计,冷凝器接受器,玻璃棒以及中学化学实验的常用仪器。1摩尔/LNaOH 溶液, 18.4 mol/LH2SO4 溶液,蒸馏水和冰
(1)补充下列实验步骤,直至达到实验目的。
第一步:组装蒸馏装置,检查其气密性;
第二步:取100 mL 废液注入250 mL 蒸馏烧瓶中,滴入1 mol/LNaOH溶液,调整废液的pH=10 ;
第三步:___________________________ 。
第四步:_______________________ 得甲醇。
第五步:__________________________得乙醇。
第六步:__________________________
得乙酸。
(2)滴入 1 mol/LNaOH 溶液,使溶液的 pH=10 的目的是______________
。
( 3 )使用 18.4 mol/LH2SO4 目的是(用化学方程式表示)_____________________ _。
9、 (5分)以下气体:①H2 ②Cl2 ③CH4 ④NO ⑤SO2 ,(烧瓶的位置不能移动)
(5分)以下气体:①H2 ②Cl2 ③CH4 ④NO ⑤SO2 ,(烧瓶的位置不能移动)
(1). 若烧瓶是干燥的,则由A口进气,可收集的气体是 ,由B口进气,可收集的气体是 。
(2). 若烧瓶内充满水,可收集到的气体是 ,气体应由 口进入(填A或B) (3). 若在烧瓶内装有一定量的溶液,用以洗气,则气体应从 口进入 (填A或B)
8、为实现我国2000年消除碘缺乏病的目标,卫生部规定食盐必须加碘,其中的碘以碘酸钾(KIO3)形式存在。已知溶液中IO3-可以与I-发生如下的反应:IO3-+5 I-+6H+ == 3I2+3H2O 据此反应,可用试剂和一些生活中常见的物质进行试验,证明在食盐在存在着IO3-。可供选用的物质是:①自来水 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④淀粉 ⑤食糖 ⑥食醋 ⑦白酒。进行上叙实验时必须使用的物质是 ( ) A、①③ B、③⑥ C、②④⑥ D、①②④⑤⑦
7、在没有现成的 CO2气体发生器的情况下,请你选用下图中的部分仪器,装配成一个简易的,能随开随用,随关随停的 CO2气体发生装置。应选用的仪器是(填入仪器的编号)。
A、abcd B、degh C、bcd D、acde
6、学生用滤纸折成一只纸蝴蝶并在纸蝴蝶上
喷洒某种试剂,挂在铁架台上。另取一只盛有某种
 液的烧杯,放在纸蝴蝶的下方(如图)。过一会儿,发现纸蝴蝶的颜色由白色纸蝴蝶上的喷洒液转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是
(
)
液的烧杯,放在纸蝴蝶的下方(如图)。过一会儿,发现纸蝴蝶的颜色由白色纸蝴蝶上的喷洒液转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是
(
)
|
|
A |
B |
C |
D |
|
纸蝴蝶上的喷洒液 |
石蕊 |
酚酞 |
酚酞 |
石蕊 |
|
小烧坏中的溶液 |
浓盐酸 |
浓氨水 |
氢氧化钠溶液 |
浓硫酸 |
5、在烧杯中加入水和苯(密度:0.88g/cm3)各50mL。将一小粒金属钠(密度:0.97g/cm3)投入烧杯中。观察到的现象可能是 ( )
A 钠在水层中反应并四处游动 B 钠停留在苯层中不发生反应
C 钠在苯的液面上反应并四处游动 D.钠在苯与水的界面处反应并可能作上、下跳动
4、某溶液含有较多的 Na2SO4 和少量的 Fe2(SO4)3 ,若用该溶液制取芒硝,可供选择的操作有:①加适量 H2SO4 溶液②加金属 Na ③结晶④加过量 NaOH ⑤加强热脱结晶水⑥过滤。正确的操作步聚是 ( )
A、②⑥③ B、④⑥①③
C、④⑥③② D、②⑥①③⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com