
题目列表(包括答案和解析)
21.(2+1+1+2=6分)虽然氟元素早在1810年就被发现,但170多年来化学家试图用化学方法制取单质氟的尝试一直未获成功。直到1985年,Karl Christe终于由氟化物制出F2。他提出的三步反应如下,请将(1)、(3)两反应配平,并填写有关空白。
(1) KMnO4+ KF+ HF+ H2O2 ==== K2MnF6+ O2+ H2O,此反应中,氧化剂是 ,氧化产物是 。
(2)SbCI5 + 5HF ==== SbF5 + 5HCI
(3) K2MnF6+ SbF5 ==== KSbF6+ MnF3+ F2
20.(2+1+1+1+2+2+1+2=12)用Na2SO3和硫粉在水溶液中加热反应,可以制得Na2S2O3,10℃和70℃时,Na2S2O3在100g水中的溶解度分别为60.0 g和212 g,常温下从溶液中析出的晶体是Na2S2O3·5H2O,Na2S2O3在酸性溶液中立即完全分解:
Na2S2O3 + 2HCI=S↓+ SO2↑+ H2O十2NaCI
现取15.1 gNa2SO3,溶于80.0 mL水。另取5.00 g硫粉,用少许乙醇润湿后(以便硫能被水浸润),加到上述溶液中,用小火加热至微沸,反应约1小时后过滤,滤液在100℃经蒸发、浓缩、冷却至10℃后析出Na2S2O3·5H2O。
(1)若加入的硫粉不用乙醇润湿,对反应的影响是 (填写选项的字母,可以多选,但选错要倒扣分)
A.会降低反应速率 B.需要提高反应温度
C.将增大反应体系的pH值 D.会减少产量
(2)反应1小时后过滤,其目的是 。
(3)滤液中除Na2S2O3和可能未反应完全的Na2SO3外,最可能存在的无机物质是 ,它是由 而产生的。如果滤液中该杂质的含量不很低,其检测的方法是
。
(4)设Na2SO3跟硫粉完全反应,当将滤液蒸发浓缩后,冷却至70℃,溶液的体积约30mL,该溶液是否达到饱和?试通过计算说明(70℃时,Na2S2O3饱和溶液的密度为1.17g/cm3)。
(5)若要计算在100℃下将溶液蒸发至体积为30.0mL,再冷却至10℃时所得到的Na2S2O3·5H2O的质量,你认为 。(填写一个选项的字母)
A.前面提供的数据已经足够
B.还需要提供100℃时溶液的密度(1.14g·cm-3)
C.还需要提供结晶后剩余溶液的体积(10.0mL)
(6)根据第(5)小题你的选择(如选A直接计算,如选B或C则可选用其数据),计算从10℃,30mL溶液中结晶而出的Na2S2O3·5H2O的质量 。
19.(2+2+3=7分)用滴管将新制的饱和氯水慢慢滴入含有酚酞的NaOH稀溶液(样品)中,当滴到最后一滴时红色突然褪去。产生该现象的原因可能有两个:
(1)是由于 ;(2)是由于 。
简述怎样用实验证明红色褪去的原因是(1)或者(2):
。
第Ⅱ卷(非选择题,共78分)
18.下列各组稀溶液,不用其它试剂或试纸,仅利用溶液间的相互反应,就不可以将它们区别开的是:
A.硝酸钾 硫酸钠 氯化铜 氯化钡
B.硫酸 硫酸铝 氯化钠 氢氧化钠
C.氯化钡 硫酸钠 碳酸钠 氢氧化钠
D.硫酸镁 碳酸钠 硫酸氢钠 氢氧化钠
普通高校招生第一次模拟试题
 化 学
化 学
考生号 姓名 区县(市)
17.已知氮的氧化物踉NaOH溶液发生的化学反应如下:
3NO2+2NaOH=2NaNO3+NO↑+H2O NO2+NO+2NaOH=2NaNO2+H2O
现有m mol NO2和n mol NO组成的混合气体,要用NaOH溶液使其完全吸收无气体剩余,现有浓度为a mol/L的NaOH溶液,则需此NaOH溶液的体积为:
A.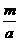 L B.
L B.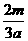 L C.
L C.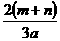 L D.
L D.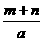 L
L
16.在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”,凡是有一个手性碳原子的物质一定具有光学活性。例如,有机化合物: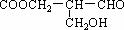 有光学活性,它分别发生下列反应:①与甲酸发生酯化反应,②与NaOH水溶液共热,③与银氨溶液作用,④在催化剂存在下与H2作用后,生成的有机物无光学活性的是:
有光学活性,它分别发生下列反应:①与甲酸发生酯化反应,②与NaOH水溶液共热,③与银氨溶液作用,④在催化剂存在下与H2作用后,生成的有机物无光学活性的是:
A.①② B.②③ C.②④ D.③④
15.下列分子中所有原子都满足最外层8电子结构的是:
A.六氟化氙 (XeF6) B.次氯酸(HClO)
C.氯化硫(S2Cl2) D.三氟化硼(BF3)
14.用高铁酸钠(Na2FeO4)对未来河湖的淡水消毒是城市饮用水处理的一种新技术,下列对Na2FeO4用于饮用水消毒处理的分析正确的是:
A.Na2FeO4在溶液中显强酸性,能消毒杀菌
B.在Na2FeO4中Fe为+6价,具有强氧化性,能消毒杀菌
C.Na2FeO4的还原产物Fe3+水解为 Fe(OH)3胶体,可使水中悬浮物凝聚沉降
D.Na2FeO4的还原产物Fe2+水解为Pe(OH)2胶体,可使水中悬浮物凝聚沉降
13.在t℃时,CuSO4的溶解度为A g,在该温度时,向(100+A) g饱和CuSO4溶液中加入A g无水CuSO4粉末后,得到一定量的蓝色CuSO4晶体。取出该晶体投入多少克水中,才能使溶液在t℃时恰好饱和:
A.100 g B.(100+A) g C.(100+2A) g D.无法计算
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com