
题目列表(包括答案和解析)
17、维生素B2也称“核黄素”,其结构如下图。维生素B2的磷酸盐衍生物是某些氧化还原酶的辅基,为生长必需物质,缺少维生素B2会引起口角炎、皮肤和眼部疾病。下列有关维生素B2的说法中正确的是 ( C )

A.核黄素晶体属于离子晶体
B. 核黄素能发生银镜反应
C. 核黄素能被酸性高锰酸钾溶液氧化
D.核黄素能与氯化铁溶液作用呈紫色
16、对于某酸性溶液(可能含有Br-、SO42-、H2SO3、NH4+),分别进行如下实验:
① 加热时放出的气体可使品红溶液褪色;
② 加入碱溶液使溶液呈碱性,再加热时放出的气体可使湿润的红色石蕊试纸变蓝;
③ 加入氯水时,溶液略呈黄色,再加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀。
对于下列物质不能确定其在原溶液中是否存在的是 ( B )
A.Br- B.SO42- C.H2SO3 D.NH4+
15、向0.1 mol / L CH3COOH溶液中加入CH3COONa晶体或加水稀释时,都会引起 ( A )
A.溶液的pH增大 B.CH3COOH的电离程度增大
C.溶液的导电能力减小 D.溶液的c(OH-)减小
14、一定条件下,可逆反应X(g)+3Y(g) 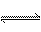 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol /L,0.3mol/ L,0.08 mol/L,则下列判断不合理的是
(C )
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol /L,0.3mol/ L,0.08 mol/L,则下列判断不合理的是
(C )
A.c1:c2=1:3 B.平衡时,Y和Z的生成速率之比为3:2
C.X、Y的转化率不相等 D.c1的取值范围为0< c1<0.14 mo /L
13、X、Y、Z、W均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的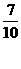 ,下列说法中正确的是
(BD )
,下列说法中正确的是
(BD )
A.阴离子的半径从大到小排列顺序为:X>Y>Z>W
B.X元素的氢化物分子间可以形成氢键
C.Y的两种同素异形体在常温下可以相互转化
D.最高价氧化物对应的水化物的酸性:W>Z
11、下列离子方程式书写正确的是 ( AD )
A.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合
Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3·H2O+H2O
B.氯化铝溶液中加入过量的氨水
Al3++4 NH3·H2O=4NH4++AlO2-+2H2O
C.向次氯酸钙溶液中通入少量的二氧化硫
Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
D.碳酸钠溶液中加入过量的苯酚
-OH+CO32-
= -O-+HCO3-
-O-+HCO3-
12 、 NA代表阿伏加德罗常数,下列说法正确的是
( B )
、 NA代表阿伏加德罗常数,下列说法正确的是
( B )
A.1L浓度为0.1 mol / L AlCl3溶液中含有的离子数是0.4NA
B. 3.9gNa2O2吸收足量的CO2时转移的电子数是0.05NA
C.标准状况下,3.2g铜与足量的浓硝酸反应生成的气体含有的分子数是0.1NA
D.标准状况下,1.12L的SO3所含的原子数是0.2 NA
|
X |
Y |
|
|
Z |
W |
10、液氨溶解金钠属后成为蓝色的导电能力很强的溶液,其颜色被认为是电子的氨合
e-(NH3)n引起的。若放置后,蓝色逐渐褪去,蒸发褪色后的溶液得到白色氨基钠(NaNH2),反应的化学方程式为:2Na+2 NH3=NaNH2+H2↑,下列说法中不正确的是 ( C)
A.溶液褪色的速率与逸出氢气的速率成正比
B.液氨中有如下平衡:2NH3=NH4++NH2-
C.液氨是一种非电解质,在水中才能电离
D.碱金属的液氨溶液是一种强还原剂
9、 实验室将NaClO3和Na2SO3按物质的量为2:1放入烧杯中,同时滴入适量H2SO4,并用水浴加热,产生棕黄色的气体X,反应后测得NaClO3和Na2SO3恰好完全反应,则X的化学式为 ( C )
A.Cl2 B.Cl2O C.ClO2 D.Cl2O3
8、下列实验方案合理的是 ( B )
A.用湿润的pH试纸测定某盐溶液的pH
B.用稀硫酸清洗长期存放氯化铁溶液的试剂瓶内壁所附着的不溶物
C.用加热法分离I2和NH4Cl 的混合物
D.为了加更快得到氢气,可以用纯锌代替粗锌
7、一定温度下,某在物质水中的溶解度为S,计算该温度下这种饱和溶液中溶质的物质的量浓度,必不可少的物理量是 ( C)
①溶液中溶质的摩尔质量②溶液中溶质和溶剂的质量比③溶液的密度④溶液的体积 A.① ② B。② ③ C.①③ D. ②④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com