
题目列表(包括答案和解析)
1.氧族元素原子结构、单质性质
|
元素名称和符号 |
氧(O) |
硫(S) |
硒(Se) |
碲(Te) |
|||||||
|
原子 结构 |
原子序数 |
8 |
16 |
34 |
52 |
||||||
|
结构示意图 |
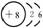 |
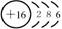 |
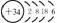 |
 |
|||||||
|
电子式 |
· · · |
· · · |
∶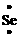 ∶ ∶ |
·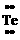 · · |
|||||||
|
主要化合价 |
-2 |
-2,+4,+6 |
-2,+4,+6 |
-2,+4,+6 |
|||||||
|
相同点 |
最外层电子数相同,都是6个电子 |
||||||||||
|
不同点 |
原子核外电子层数不同,依次增大 |
||||||||||
|
原子半径 |
 |
||||||||||
|
物 理性 质 |
颜色和状态 |
无色无味气体 |
淡黄固体 |
灰色固体 |
银白色固体 |
||||||
|
密度 |
 |
||||||||||
|
熔点(℃) |
 |
||||||||||
|
沸点(℃) |
 |
||||||||||
|
水、有机溶剂溶解度 |
 |
||||||||||
|
化学反 |
与金属反应 |
易与金属反应 |
易与金属反应 |
反应较难 |
多数不反应 |
||||||
|
与非金属反应 |
易与H2、C、P、S等反应 |
能与H2、C、O2反应 |
反应难 |
一般不反应 |
|||||||
|
与化合物反应 |
能与许多物质反应 |
能与氧化性酸、强碱反应 |
反应少 |
反应很少 |
|||||||
5.掌握离子反应、离子反应发生的条件及离子方程式的书写。
4.了解硫酸的性质、用途及硫酸根离子的检验;了解几种常见的硫酸盐。
3.掌握工业上接触法制硫酸的反应原理及有关的多步反应的计算;
2.了解硫的氧化物对环境的污染及环境保护的意义;
1.以硫元素为代表,了解氧族元素的单质、氢化物及其氧化物的重要性质;理解氧族元素的性质递变规律;
12.对某宇航员从天外某星球空间取回的样品进行如下实验:①将气体样品溶于水发现其主 要成分A易溶于水;②将A的浓溶液与MnO2共热生成一种黄绿色单质气体B,B通入NaOH溶液 中生成两种钠盐;③A的稀溶液与锌粒反应生成气体C,C与B组成的混合气体经光照发生爆炸 ,生成气体A,实验测得反应前后气体体积不变。据此回答下列问题:
(1)写出A、B、C的化学式A 、B 、C ;
(2)写出A的浓溶液与MnO2共热的化学方程式 ;
(3)写出B通入NaOH溶液生成两种钠盐的化学方程式 ;
(4)科研资料表明:如果该星球上有生命活动,则这些生物可能从该星球上液态氨的海洋中产生,因为那里的液氨相当于地球上的水。据此推测:该星球上是否有生命活动?简述理由。
知识点:考查氯气、氯化氢的性质。
能力点:发散思维的能力。
11.工业上制备单质碘的方法之一是从碘酸盐开始的。第一步先用适量的亚硫酸氢盐将碘酸
盐还原成碘化物,离子方程为:IO3-+HSO3- I-+SO42-+H+。第二步将第一步得到的酸性碘化物溶液再跟适量的碘酸盐溶液混合,发生反应析出了碘。试问:(1)第二步发生反应的离子方程式是
。
I-+SO42-+H+。第二步将第一步得到的酸性碘化物溶液再跟适量的碘酸盐溶液混合,发生反应析出了碘。试问:(1)第二步发生反应的离子方程式是
。
(2)若要使碘酸盐的利用率最高,碘酸盐在第一步和第二步反应中的用量之比应为 。
知识点:单质碘的制备方法。
能力点:知识的迁移能力。
10.饱和氯水长期放置后,下列微粒在溶液中不减少的是( )
A.Cl2 B.HClO C.Cl- D.H2O
知识点:次氯酸见光易分解及氯气与水的反应
能力点:分析问题的能力
9.向NaBr、NaI的混合溶液中通入足量Cl2之后加热,将溶液蒸干,并灼烧片刻,最后残留的物质是( )
A.NaCl B.NaCl、NaBr、NaI
C.NaBr、NaI D.NaCl、I2
知识点:氯气的氧化性及单质溴、碘的物理性质。
能力点:分析问题的能力。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com