
题目列表(包括答案和解析)
20.将amol H2S和1mol O2置于一个容积可变的容器内进行反应。维持容器内气体的压强不变(101KPa),在120℃下测得反应前后容器内气体的密度分别为d1和d2。若a的取值不同,则H2S的氧化产物可能有如下三种情况:
(1)全部是SO2,此时a的取值范围是 。
(2)全部是S,此时a的取值范围是 ,并且d1 d2(填“小于”、“大于”或“等于”)。
(3)部分是SO2,部分是S,此时a的取值范围是 。反应所生成SO2的物质的量为 mol。容器内气体的物质的量之和为 mol(以含a的代数式表示)。
考查目的:H2S气体的燃烧问题是一个考试热点,完成本题要对H2S燃烧原理、条件非常熟练。考查学生的综合解题能力。
19.有一瓶亚硫酸钠溶液已部分氧化变质:2Na2SO3+O2 2Na2SO4,某学生
设计了下列实验,确定Na2SO3的纯度:
2Na2SO4,某学生
设计了下列实验,确定Na2SO3的纯度:
①称取ag样品。称量时所用主要仪器的名称是
②样品的溶解。溶解过程中使用玻璃棒搅拌的目的
③在溶液中加入过量的BaCl2溶液且用盐酸酸化。
(1)为什么要用盐酸酸化?
(2)BaCl2为什么要过量?
(3)怎样检验BaCl2溶液是否过量?
(4)为什么要洗涤沉淀?
(5)怎样洗涤沉淀?
(6)怎样判断沉淀是否洗净?
(7)烘干沉淀并计算。烘干后称量沉淀质量为bg,列出计算Na2SO3纯度的计算式。
考查目的:这是一道综合实验题,要回答完整本题必须对这个实验有一条清晰的实验方案, 考查实验能力。
18.某无色溶液可能含有下列钠盐中的几种:(A)氯化钠 (B)硫化钠 (C)亚硫酸钠 (D)硫 代硫酸钠 (E)硫酸钠 (F)碳酸钠。向此溶液中加入适量稀硫酸,有浅黄色的沉淀析出,同 时有气体产生。此气体有臭鸡蛋气味,可使澄清的石灰水变浑浊,不能使品红试液褪色。根 据上述实验现象回答下列问题。
(1)不能使品红试液褪色,说明该气体中不含 (填分子式) 。
(2)此无色溶液中至少存在哪几种钠盐?请写出全部可能的情况(填写相应的字母)。
第一种情况是 ,第二种情况是 ,第三种情况是
,第四种情况是 。(可不填满,也可补充)
考查目的:有关硫的化合物的知识和思维能力。
17.将0.8g某种铁的硫化物在O2流里灼烧,使硫全部氧化为二氧化硫,再将所得的SO2通过氧化剂使之全部转化为三氧化硫,并与水化合完全转化为硫酸。这些硫酸恰好与40ml0.5 mol/L NaOH溶液中和,则某种铁的硫化物中含硫的质量分数 。
考查目的:这是一道多步反应的计算题,只要从多步反应中找出需要的关系式,便能解答。 训练学生的归纳、分析能力。
16.氯酸钾和亚硫酸氢钠间氧化还原反应生成Cl-和S+6的速度,如下图所示,又已知这个反应的速度随着溶液中氢离子浓度增大而加快。
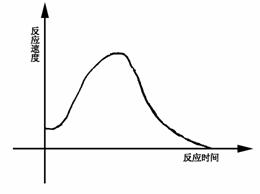
(1)为什么反应开始时反应速度加快?
(2)为什么后期反应速度下降?
考查目的:本题涉及的知识是氧化还原反应,仔细分析反应式,是能回答问题的,考查分析问题能力。
15.摄影工艺中的废定影液的PH值小于7,其中含有银的复杂化合物,为了回收银,进行如下操作:向盛有定影液的烧杯中,加入少量稀NaOH溶液,再加入硫化钠溶液,生成黑色沉淀。过滤,将固体移入坩埚中加碳酸钠和硼砂(催化剂)混合加热,放出二氧化碳和氧气。将残留的固体用水洗涤,即得到固体银,而洗涤液中主要含有硫化钠,试回答下列问题:(1)开始时为何要向废液中加入少量氢氧化钠溶液?(2)过程中的黑色沉淀物质是什么?(3)写出加热时坩埚内发生的反应的化学方程式。
考查目的:这是一道信息题,用学习过的化学知识解释实际问题,培养学生解决实际问题的 能力。
14.亚硫酸钠中有+4价的硫,它既有氧化性又有还原性。现有试剂:溴水、硫化钠溶液、亚 硫酸钠溶液、稀硫酸、烧碱溶液、氨水。
①要证明Na2SO3具有还原性,应选用的试剂有 ,看到的现象 ,反应的离子方程式为 。
②要证明Na2SO3具有氧化性,应选用的试剂有 、 看到的现象 ,反应的离子方程式为
考查目的:这道题要用到的知识有+4价硫的氧化还原性,氧化还原反应发生的条件及现象, 离子方程式的书写等,是一道综合题,考查学生的综合思维能力。
13.接触法制硫酸排放的尾气中含有少量的SO2,为防止污染大气,排放前应进行尾气处理,使其得到综合利用。
(1)某硫酸厂每天排放5000m3(标况)尾气,其中SO2的体积分数为0.2%,若用NaOH溶液、石灰及氧气等物质处理,假设硫元素不损失,理论上可得到多少千克石膏(CaSO4·2H2O )?
(2)如果将一定体积的尾气通入200mL2 mol·L-1的NaOH溶液中,使其完全反应,经测定所得溶液含33.4g溶质,试分析溶液的成分,并通过计算确定各成分的物质的量。
考查目的:SO2的处理与回收,培养学生的环保意识。
12.固体A、B都由两种相同的元素组成。在A、B中两种元素的原子个数比分别为1∶1和1∶2。将A和B在高温时燃烧,产物都是C(固体)和D(气体)。由D最终可制得E(酸),E和另一种酸 组成的混酸常用于制取有机炸药。E的稀溶液和A反应时,生成G(气体)和F(溶液),G通入D的 水溶液,有浅黄色沉淀生成。在F中滴入溴水后,加入氢氧化钾溶液,有红褐色沉淀生成, 该沉淀加热时又能转变为C。根据上述事实回答:
(1)A的化学式是 ,B的化学式是 。
(2)写出下列反应的化学方程式。
①B煅烧生成C和D ②G通入D溶液中 ③在F中滴入溴水 ④A和E的反应
考查目的:硫的化合物的一些性质以及学生综合推理能力。
11.下列各组离子在水溶液中能大量共存的是( )
A.CO2-3、HCO-3、OH-、Na+
B.K+、Cl-、S2-、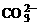
C.H+、Br-、Na+、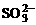 D.Ba2+、Cu2+、NO-3、
D.Ba2+、Cu2+、NO-3、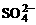
考查目的:离子能否共存就是看这些离子在溶液中能否发生反应(复分解反应、氧化还原反应),本题对学生分析能力进行考查。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com