
题目列表(包括答案和解析)
3、在同温同压下,合成氨反应N2+3H2=2NH3进行到某时刻达到平衡.起始时N2和H2共120体积,平衡时总体积为70体积,则原混合气体中N2和H2的体积比可能为:
A、1:3;B、9:15;C、5:19;D、1:1。
2、某无色透明的碱性溶液中可能大量共存的离子组为:
A、K+,NH4+,Cl-,NO3-;B、Na+,K+,HCO3-,SO42-;
C、K+,Na+,NO3-,MnO4-;D、Na+,S2-,SO32-,Cl-。
1、X元素的最高正价与负价的代数和为6,Y离子和X离子相同的电子层结构,且能按1:2组成化合物Z,则Z可能为:A、CaCl2;B、MgF2;C、Na2O;D、K2S。
26、(10分)某化工厂每小时生产98%(质量分数)硫酸at,为使硫充分燃烧,且在下一步催化氧化时不再补充空气,要求燃烧后的混合气体中含氧气的体积分数为b%。若空气中氧气的体积分数为21%,且不考虑各生产阶段的物料损失,试计算:
(1)该厂每小时消耗标准状况下空气的体积为多少m3?
(2)为满足题设要求,b%的下限是多少?
25、(5分)标准状况下,用一定量的水吸收氨气后制得浓度为12.0mol/L、密度为0.915g/mL的氨水。试计算1体积水吸收多少体积的氨气可制得上述氨水。
(本题中氨的式量以17.0计,水的密度以1.00g/mL计)
24、(8分)A、B都是芳香族化合物,1molA水解得到1molB和1molC醋酸。A、B的分子量都不超过200,完全燃烧都只生成CO2和H2O,且B分子中碳和氢元素总的质量分数为65.2%。A溶液具有酸性,不能使FeCl3溶液显色。
(1)A、B分子量之差是 。(2)1个B分子中应该有 个氧原子。
(3)A的分子式是 。(4)1molB最多消耗NaOH mol。
23、(14分)有机物J(C19H20O4)不溶于水,毒性低,与聚氯乙烯、聚乙烯等树酯具有良好的相溶性,是塑料工业的主要增塑剂,可用下列方法合成之。

(1)②的反应类型 ,②的反应条件 ,④的反应类型
(2)写出结构简式:Y ,F 。
(3)B+E→J的化学方程式
(4)写出E的属于芳香烃衍生物的同分异构体的结构简式:
, , 。
(5)G有很多同分异构体,含有酯基和一取代苯结构的就有五个,其中三个是:
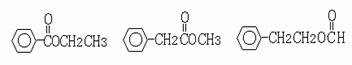
请写出另外两个同分异构体的结构简式: , 。
22、 (10分)如图所示,已知:
(10分)如图所示,已知:
(1)甲、乙、丙、丁均为前三周期元素的单质。
(2)在一定条件下甲与丙和甲与丁都按物质的量之比为1:3反应,分别生成X和Y,在产物中元素甲呈负价。
(3)在一定条件下乙与丙和乙与丁都按物质的量之比1:2反应,分别生成Z和W,在产物中元素乙呈负价。
请填空:
(1)甲是 ,乙是
(2)甲与丙反应生成X的化学方程式是
(3)乙与丁反应生成W的化学方程式是
21、(8分)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境中排放有害物质。例如:
|





(1)在上述有编号的各步中,需用还原剂的是 ,需用氧化剂的是 。
(2)在上述循环中,既能与强酸反应又能与强碱反应的两性物质的化学式是 。
(3)①步的化学方程式如下,请完成配平,并标出电子转移的方向和数目
 ( )Na2Cr2O7+( )KI+( )HCl --( )CrCl3+(
)NaCl+( )KCl+( )I2+( )
( )Na2Cr2O7+( )KI+( )HCl --( )CrCl3+(
)NaCl+( )KCl+( )I2+( )
20、(10分)第19题的实验结束时,老师让学生思考残留固体的利用方案。有学生提出,若前面实验中KClO3都已完全分解,则可用该残渣为原料制取氯化氢气体。
(1)对此他设计的实验步骤依次是:溶解、蒸发、结晶、制取气体。其中缺少的必要步骤是 。
(2)他开出的实验仪器和用品是:烧杯、烧瓶、蒸发皿、量筒、集气瓶、分液漏斗、酒精灯、药匙、托盘天平、铁架台、铁夹、铁圈、双孔橡皮塞、玻璃导管、火柴、蒸馏水、橡皮管。所缺少的必要试剂是 ,还缺少的必要的实验仪器用品是
。
(3)请你再提出一种该残留固体的利用方案:用该残留固体和 (一种必要的物质的名称)为原料制取 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com