
题目列表(包括答案和解析)
9、下列离子方程式书写正确的是
(A)向含有0.1mol
NaOH溶液中通入3.36L(标况)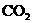 气体
气体
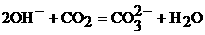
(B)向100mL 0.1mol/L Fe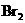 溶液中通入0.025mol的
溶液中通入0.025mol的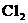
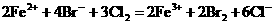
(C)硫酸氢钠与足量的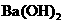 溶液反应
溶液反应
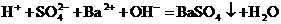
(D)碳酸氢镁溶液与足量的NaOH溶液反应
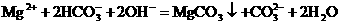
8、有关叙述:(1)非金属单质M能从N的化合物中置换出非金属单质N。(2)M原子比N原子容易得到电子。(3)单质M跟H2反应比N跟H2反应容易得多。(4)气态氢化物水溶液的酸性HmM>HnN。(5)氧化物水化物的酸性HmMOx>HnNOy。(6)熔点M>N。能说明M比N的非金属性强的叙述是
A.①②③ B.②③⑤ C.①②④⑤ D.全部
7、今有甲、乙、丙三瓶等体积的新制氯水,浓度均为0.1 mol·L-1。如果在甲瓶中加入少量的NaHCO3晶体(mmol),在乙瓶中加入少量的NaHSO3晶体(mmol),丙瓶不变。片刻后,甲、乙、丙三瓶溶液中HClO的物质的量浓度大小关系是(溶液体积变化忽略不计)
A.甲=乙>丙 B.甲>丙>乙
C.丙>甲=乙 D.乙>丙>甲
6、在含有FeBr2和FeI2的混合溶液中通入足量的氯气,然后把溶液蒸干,并将残渣灼烧,得到的残渣是
A.FeCl2、Br2、I2 B.FeCl3、I2 C.Fe(OH)3、I2 D.Fe2O3
5、氯化溴(BrCl)和Br2、Cl2具有相似的性质,下列有关氯化溴性质的判断中错误的是
A、在CCl4中的溶解性BrCl<Br2
B.、BrCl氧化性比Br2强,比Cl2弱
C.、沸点BrCl>Br2 D.常温下BrCl可与NaOH溶液反应生成NaCl和NaBrO
4、某温度下,w g某物质在足量氧气中充分燃烧,其燃烧产物立即与过量的Na2O2反应,固体质量增加w g。在①H2②CO ③CO和H2的混合气 ④HCHO ⑤CH3COOH
⑥HO-CH2-CH2-OH中,符合题意的是
A.均不符合 B.只有①②③ C.只有④⑤ D.全部符合
3、下列各项的叙述中都包含两个数值,前一数值大于后一数值的是( )
(A)单质碘中的分子间作用力和干冰中的分子间作用力
(B)NaCl晶体中与一个Cl-紧邻的Na+数和CsCl晶体中与一个Cl-紧邻的Cs+数
(C)晶体硅中Si-Si键的键能和金刚石中C-C键的键能
(D)氨分子中N-H键的键角和甲烷分子中C-H键的键角
2、已知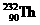 (钍)原子可发生下列放射性衰变:
(钍)原子可发生下列放射性衰变: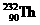
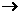
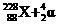 ,生成的元素与Fr(钫)处于同一周期,以下关于X的推断中错误的是( )
,生成的元素与Fr(钫)处于同一周期,以下关于X的推断中错误的是( )
(A)X的氢氧化物是一种强碱 (B)X的碳酸正盐不溶于水
(C)X的原子核外有6个电子层 (D)X的最高化合价为+2价
1、据悉,用10 B合成10 B20有非常好的抗癌、治癌作用,下列说法正确的是
A.10 B 和10B20互为同位素 B.10B和10B20 互为同系物
C.10B的中子数与核外电子数相等 D.10B20是一种熔点很高,硬度很大的物质
25(5分)、把0.69gNa投入500mL0.1mol/L的AlCl3溶液中,有0.78g白色沉淀生成,再投入多少克Na可使沉淀恰好完全溶解?
26、(9分)在标准状况下,将224 L HCl气体溶于635 mL水中(ρ=1 g/cm3),所得盐酸的密度为1.18 g/cm3。试计算:
(1) 取出这种盐酸100.0 mL,稀释至1.18 L,所得稀盐酸的物质的量浓度。
(2)在40.0 mL 0.0650 mol·L-1Na2CO3溶液中,逐滴加入(1)所配制的稀盐酸,边滴边振荡。若使反应不产生CO2气体,加入稀盐酸的体积最多不能超过多少毫升?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com