
题目列表(包括答案和解析)
21. (8分)
⑴ D是Al2O3(2¹) H是H2(2¹)
⑵①Al3++3H2O
(8分)
⑴ D是Al2O3(2¹) H是H2(2¹)
⑵①Al3++3H2O  Al(OH)3-+3H+ (不用不给分。不配平或不注明反应条件或条件注明错误的只给1分,下同) (2¹)
⑶3Fe+4H2O Fe3O4+4H2↑(2¹)
Al(OH)3-+3H+ (不用不给分。不配平或不注明反应条件或条件注明错误的只给1分,下同) (2¹)
⑶3Fe+4H2O Fe3O4+4H2↑(2¹)
20.(12分) ⑴AG (颠倒顺序不给分)(2¹) ④⑦①②(少一个不给分)(2¹) ⑵抑制NH·HO的电离和氨的溶解,使氨从溶液中逸出。(2¹)能 (1¹) ⑶F(1¹) NH3、Cl2、HCl中的一种或Cl2和HCl(2¹)⑤②(或⑥)(2¹)
19.不合理。估算所得溶液中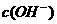 约为
约为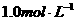 ,故在酚酞呈红色的范围内
,故在酚酞呈红色的范围内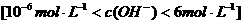 。
。
26.为了防治环境污染并对尾气进行综合处理,某硫酸厂用氨水吸收尾气中的SO2,再向吸收液中加入浓硫酸,以制取高浓度的SO2及(NH4)2SO4和NH4HSO4固体。为测定上述(NH4)2SO4和NH4HSO4固体混合物的组成。现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[(NH4)2SO4和NH4HSO4分解温度均高于200℃],测得有关数据如下(标准状况):
|
实验序号 |
样品质量/g |
NaOH溶液体积/mL |
氨气体积/L |
|
I |
7.4 |
40.00 |
1.68 |
|
II |
14.8 |
40.00 |
3.36 |
|
III |
22.2 |
40.00 |
1.12 |
|
IV |
37.0 |
40.00 |
0.00 |
(1) 实验过程中有关的离子反应方程式为
(2)由I组数据直接推测:标准状况下3.7g样品进行同样实验时,生成氨气的体积为 L
(3)试计算该混合物中的(NH4)2SO4和NH4HSO4物质的量之比
(4)欲计算该NaOH溶液物质的量浓度应选择第 组数据,其浓度为 。
25.A为烃,B为烃的含氧衍生物,由等物质的量的A和B组成的混合物0.05mol在0.125molO2中完全燃烧生成0.1molCO2和0.1mol H2O ,通过计算回答:
(1)从分子组成的角度分析,该混合物的组合可能有几种?
(2)另取一定量的A和B的混合物完全燃烧,将其以任意比混合且物质的量和一定。
①若耗氧一定,则A和B的分子式分别是 、 。
②若生成CO2和H2O的物质的量一定,则A和B的分子式分别是 、 。
24.已知有两种有机反应:
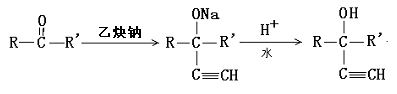 ①
①
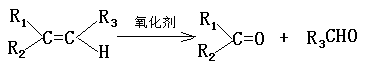 ②
②
现有化合物A的一系列反应,起始物为只有一个侧链的芳香烃(某些反应的条件已略去)

试回答:
(1)A的结构简式是
(2)反应过程中属于加成反应的是(填编号):
(3)写出下列反应的化学方程式:
B+E→G
E→F
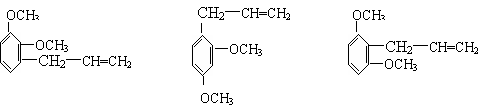
23.(9分)下列三种有机物都是某些植物挥发油中的主要成分。
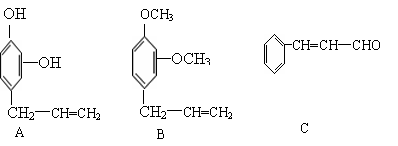
回答下列问题 ⑴这三种有机物均属于(选填字母)______ a 芳香烃 b 酚类 c 芳香族化合物 d 醛类 ⑵A能发生的反应类型(选填字母)_____ a、消去 b、与氢氧化钠溶液中和 c、加成反应 d、氧化反应 e、加聚反应 f、还原反应 ⑶一定质量的有机物C,在足量的O2中完全燃烧,生成CO2和消耗O2的物质的量之比为_____ ⑷B分子有多种同分异构体,其中均含有两个“-OCH3”和一个“-CH2-CH=CH2”基
团的芳香族化合物有五种,请写出其余两种的结构简式:______________、
______________________
22.(10分)在一固定容积的密闭容器中,保持一定的温度,在一定的条件下进行以下的反应:A(g)+2B(g)  3C(g),已知加入1molA和3molB且达到平衡时生成amolC.
3C(g),已知加入1molA和3molB且达到平衡时生成amolC.
⑴达到平衡时,C在反应混合气体中的物质的量百分含量为__(用含a的关系式表示)
在相同实验条件下,若在同一容器中改为加入2molA和6molB,达到平衡后,C的物质的量为___(用含a的关系式表示),此时C在反应混合气体中的物质的量百分含量_____(填增大、减小、不变)
⑶在相同实验条件下,若在同一容器中改为加入2molA和8molB,若要求平衡后,C在反应混合气体中的物质的量百分含量不变,还应加入C___mol。
⑷若在同一容器中,加入nmolA和3nmolB,则平衡时C的物质的量为mmol。若改变实验条件,可以使C的物质的量在m-2m之间变化,那么,n的取值范围是____(用字母m、n关系式表示)。
21.(8分)已知A-K所代表的各物质都是中学化学里常见的物质,且I是具有磁性的物质,D和K都具有两性。一定条件下,各物质间的相互反应转化关系如下图所示:
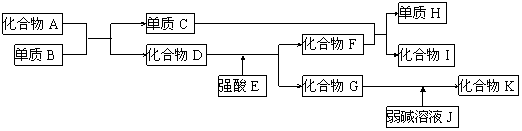
请回答:⑴写出有关物质的化学式:D是_____,H是________。
⑵写出下列反应的化学方程式:
① 化合物G的溶液不呈中性,其原因用离子方程式表示为______________
② C+F→H+I________________________________。
19.已知:⑴溶液中c(OH-)10-6mol·L-1和6 mol·L-1之间,可使无色的酚酞试液呈红色;⑵过氧化氢具有漂白性。
据此回答下列问题:
现将0.39g过氧化钠粉末溶解在10mL水中,向所得溶液中加入2滴酚酞,放置片刻,红色褪去。
⑴甲同学认为红色褪去的原因是由于溶液中c(OH-)较大,此种说法
(填“正确”或“不正确”),通过估算说明理由 ;
⑵乙同学认为红色褪去的原因可能是由于反应中有过氧化氢生成,此种说法
(填“正确”或“不正确”),并通过①分析推理、②提出假设、③设计实验来说明理由。
①分析推理 ;
②提出假设 ;
③设计实验
。
20某学生拟利用下列两个在室温下能顺利进行的反应,在实验室制取少量纯净的氮气。
3Cl2+2NH3=N2+6HCl NH3·H2O(浓) NH3↑+H2O
实验时,可供选择的仪器装置如下图所示。

实验时可供选择的试剂有:①饱和食盐水,②浓硫酸,③浓硝酸,④浓盐酸,⑤稀烧碱溶液,⑥碱石灰,⑦二氧化锰粉末,⑧浓氨水。
该生设计的实验流程是:

回答下列问题:
⑴在所给出的仪器装置中,要组装成制得纯净的氨的装置,按实验时装置合理连接的先后顺序应依次选取_______(填图中仪器装置的代号);制得纯净的氯气选用的试剂是_________(填试剂的编号)。 ⑵利用浓氨水和氢氧化钠固体制氨时,氢氧化钠固体的作用是__________;此时若用碱石灰代替氢氧化钠,能否达到目的?_____。 ⑶氯气跟氨的反应应在装置__________(填装置代号)中进行,生成的氮气中可能会混有的杂质气体有______________________;若生成的氮气中混有氯气或氯化氢气体,则净化时先后依次通过的试剂是__________(填试剂的编号)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com