
题目列表(包括答案和解析)
17、通常状况下,NC13是一种油状液体,其分子空间构型与氨分子相似,下列对NC13的有关叙述正确的是
A.分子中N-C1键键长比CCl4分子中C-C1键键长长
B.分子中的所有原于均达到8电子稳定结构
C.NCl3分子是非极性分子 D.NBr3比NCl3易挥发
16、我国首创的铝-空气-海水电池被称为“海洋电池”,是一种无污染的长效电池,以铁铂合金网(接触空气)和铝分别为电池的两极放入海水中即可供电,下列反应与该电池的工作原理有关的是
① Fe-2e-===Fe2+ ②Al-3e- ===A13+ ③O2+2H2O+4e- ===4OH-
④4Al+3O2+6H2O===4Al(OH)3 ⑤2Fe+O2+2H2O===2Fe(OH)2
A.②③④ B.①③⑤ C.①⑤ D.③④
15、.已知A2O 可与B2-反应,B2-被氧化,产物为B单质,A2O
可与B2-反应,B2-被氧化,产物为B单质,A2O 被还原,产物为A3+,且知100
mL c(A2O
被还原,产物为A3+,且知100
mL c(A2O )=0.3mol·L-1的溶液与150
mL c(B2-)=0.6mol·L-1的溶液恰好完全反应,则n值为
)=0.3mol·L-1的溶液与150
mL c(B2-)=0.6mol·L-1的溶液恰好完全反应,则n值为
A.4 B.5 C.6 D.7
14、1999年曾报道合成和分离了含高能量的正离子N 的化合物N5AsF6,下列叙述中错误的是
的化合物N5AsF6,下列叙述中错误的是
A.N 共有34个核外电子
B.N
共有34个核外电子
B.N 中氮-氮原子间以共用电子对结合
中氮-氮原子间以共用电子对结合
C.化合物N5AsF6中As化合价为+1 D.化合物N5AsF6中F的化合价为-1
13、已知甲、乙溶质质量分数与密度的关系如下表:
|
溶质质量分数 |
甲溶液密度(g/cm3) |
乙溶液密度(g/cm3) |
|
1% |
0.95 |
1.02 |
|
5% |
0.92 |
1.04 |
|
10% |
0.90 |
1.07 |
甲物质的1%的溶液与9%的溶液等体积混合,乙物质的1%的溶液与9%的溶液等体积混合后,下列叙述正确的是
A.混合后甲、乙溶液质量分数均大于5%
B.混合后乙溶液质量分数大于5%,甲溶液质量分数小于5%
C.混合后甲溶液质量分数大于5%,乙溶液质量分数小于5%
D.混合后甲、乙溶液质量分数均等于5%
12、m g H2和n g He的下列说法中,正确的是
A.同温同压下,H2与He的体积比为m∶2n
B.同温同压下,若m=n,则H2与He的分子数之比为2∶1
C.同温同压下,同体积时,H2与He的质量比m/n>1
D.同温同压下,H2与He的密度比为1∶2
11、已知锂及其化合物的许多性质与碱金属差异较大,却与镁相似。下面有关锂及其化合物性质的叙述不正确的是
A.锂在过量氧气中燃烧主要产物是氧化锂而不是过氧化锂
B.碳酸锂受强热很难分解
C.碳酸锂的溶解度比碳酸氢锂的大
D.锂可以与氮气化合生成氮化锂(Li3N)
10、设No为阿伏加德罗常数的值,下列正确的是
A.使Na2O2与H2O反应生成常温常压下16g的O2气体,反应中转移的电子数No
B.使22.4L的HCl气体溶于水,水中H+ 数为No
C.使1molCO2与过量NaOH溶液反应后,溶液中CO32- 个数约No
D.3g金刚石中所含有共价键数目为No
9、下列离子方程式书写正确的是
(A)向含有0.1mol
NaOH溶液中通入3.36L(标况) 气体
气体

(B)向100mL 0.1mol/L Fe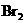 溶液中通入0.025mol的
溶液中通入0.025mol的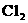

(C)硫酸氢钠与足量的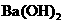 溶液反应
溶液反应
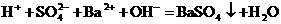
(D)碳酸氢镁溶液与足量的NaOH溶液反应
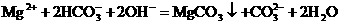
8、有关叙述:(1)非金属单质M能从N的化合物中置换出非金属单质N。(2)M原子比N原子容易得到电子。(3)单质M跟H2反应比N跟H2反应容易得多。(4)气态氢化物水溶液的酸性HmM>HnN。(5)氧化物水化物的酸性HmMOx>HnNOy。(6)熔点M>N。能说明M比N的非金属性强的叙述是
A.①②③ B.②③⑤ C.①②④⑤ D.全部
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com