
题目列表(包括答案和解析)
3.下列有关金属元素特征的叙述正确的是 ( )
A.金属元素的原子只有还原性而离子只有氧化性
B.金属元素的音质在常温下均为固体
C.金属元素在不同化合物中化合价均相同
D.金属元素在化合物中一定显正价
2.下列关于“生活中的化学”的叙述中不正确的是 ( )
A.棉花和蚕丝的主要成分都是纤维素
B.误食重金属盐,立即喝牛奶或生蛋清进行解毒
C.食用植物油的主要成分是高级不饱和脂肪酸甘油酯,是人体的营养物质
D.新居室内装饰材料中缓慢释放出的甲醛、甲苯等有机物会污染室内空气
1.1993年的世界10大科技新闻称,中国学者徐志傅和美国科学家穆尔共同合成了世界上最
大的碳氢分子,其中一个分子由1134个碳原子和1146年氢原子构成。关于此物质,下列
说法错误的是 ( )
A.属于烃类化合物 B.具有类似金刚石的硬度
C.在常温下呈固态 D.能在空气中燃烧
26、常温下,用惰性电极电解1L 1.35mol/L的硫酸铜溶液,在电路中通过0.5mol电子后,将电极反接,又通过1mol电子,此时假设溶液体积不变,求:
(1)第二次通电后溶液中各离子的物质的量浓度。
(2)若通电前测得溶液密度d=1.2g/cm3,在第二次通电后溶液中CuSO4的质量分数。
25、据报道,最近摩托罗拉(MOTOROLA)公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量是现用镍氢电池和锂电池的10倍,可连续使用1个月才充电一次。假定放电过程中,甲醇完全氧化产生的二氧化碳被充分吸收生成CO32-。
(1)该电池反应的总离子方程式为 ,
(2)甲醇在 极发生反应(填“正”或“负”),电池中放电过程中溶液的pH将 (填“下降”、“上升”或“不变”);若有16克甲醇蒸气被完全氧化产生电能,并利用该过程中释放的电能电解足量的硫酸铜溶液,假设能量的利用率为80%,则将产生标准状况下 的氧气 L。
(3)最近,又有科学家制造出一种固体电解质的燃料电池,其效率更高。一个电极通入空气,另一个电极通入汽油蒸汽。其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-离子(其中氧化反应发生完全)。以丁烷代表汽油。
a/电池的正极反应式为 ;
b/放电时固体电解质里的O2-离子的移动方向是向 极移动(填“正”或“负”)。
24、已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有如下关系:(1)c(Cl-)>c(NH4+)>c(H+)>c(OH-)
(2)c(Cl-)>c(NH4+)> c(OH-)> c(H+)
(3)c(NH4+)> c(Cl-) >c(OH-)>c(H+)
(4)c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白
a/若溶液中只溶解了一种溶质,则该溶质是 ,上述四种离子浓度的大小顺序
关系为 。(填序号)
b/若上述关系中(3)是正确的,则溶液中的溶质为 ;
若上述关系中(4)是正确的,则溶液中的溶质为 。
c/若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前
c(HCl) c(NH3•H2O)(填“<”、“>”、或“=”,下同),混合前酸中c(H+)和碱中c(OH-)的关系c(H+) c(OH-)。
23、某二元酸H2A在水中的电离方程式为:H2A=H++HA-,HA-≒H++A2-,回答下列问题:
(1)Na2A溶液显 性,理由是(用离子方程式表示) ;
(2)若0.1mol/LNaHA溶液的pH=2,则0.1mol/LH2A溶液中C(H+)可能是 0.11mol/L
(填<、=、>),理由是 。
(3)0.1mol/LNaHA溶液中各种离子浓度由大到小的顺序是
。
22、如图中每一方框中的字母代表一种反应物或生成物。已知A、B、C、D均为前三周期元素的单质,也是中学化学常见的物质。其中A、B为固体,且B是良好的半导体材料;C、D为气体。电解H的饱和溶液生成X、C和D,此反应是一个重要的化工反应。(物质间相互转化时水已略去)
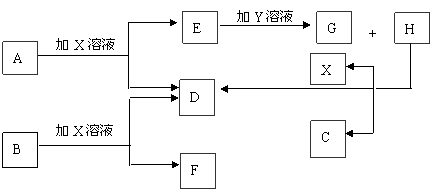
请填空:
(1)写出下列物质的化学式:
A C X 。
(2)B单质为 晶体(填晶体类型)
(3)E和G在水溶液中混合反应的离子方程式为 ;
(4)25℃时,用石墨电极电解含0.4molH物质的水溶液,在阳极产生0.1mol气体,测得此
时溶液体积为200mL,则此时该溶液的pH约为 。
21、NH4Cl和C2H5Br都能与水发生水解反应,反应中H2O分子按两种方式离解:
a离解成氢离子(H+)和氢氧根离子(OH-)
b离解成氢原子(H)和羟基(-OH)
(1)NH4Cl水解的化学方程式 ,
水的离解方式 (填字母代号,下同);C2H5Br水解化学方程式
,水的离解方式 。
(2)Mg4C3的水解按“a”式进行,化学方程式 。
(3)PCl3的水解按“b” 式进行,化学方程式 。
20、用下图所示装置(酒精灯、铁架台等未画出)制取三氯化磷,在烧瓶d中放入足量白磷,将氯气迅速而又不间断地通入d中,氯气与白磷发生反应,产生火焰。
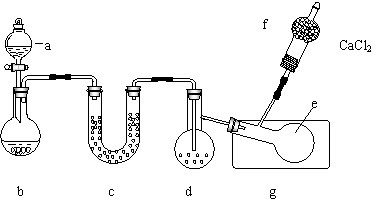
PCl3与PCl5物理常数如下:
|
|
熔点 |
沸点 |
|
PCl3 |
-112℃ |
76℃ |
|
PCl5 |
148℃ |
200℃(分解) |
图中a、b应该装入的试剂或药品分别是浓盐酸和MnO2,并在b仪器处加热。请据此回答下列问题:
(1)在蒸馏烧瓶e中收集生成的PCl3,为保证PCl3蒸气冷凝,应在水槽g中加入 。
(2)PCl5遇水蒸气强烈水解,甚至发生爆炸,所以d、e仪器及装入其中的物质都不能含
有水分。为除去氯气中的水分,c中应装入 作干燥剂。
(3)实验室将白磷保存于水中,取出的白磷用滤纸吸干表面水分,浸入无水酒精中片刻,
再浸入乙醚中片刻即可完全除去水分。用上述方法除去水分的原因是
。
(4)为防止氯气污染空气,装置未端导出的气体应如何净化处理 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com