
题目列表(包括答案和解析)
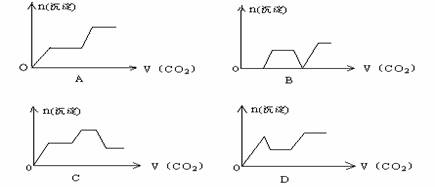
7、将足量的CO2不断通入KOH、Ca(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为:
6、科学家预言超级原子的发现将会重建周期表,2005年1月美国科学家在《Science》上发表论文,宣布发现A1的超原子结构A113和A114,并在质谱仪检测到稳定的Al13I-等。A113、A114的性质很象现行周期表中的某主族元素,已知这类超原子当具有40个价电子时最稳定。下列说法不正确的是
A、All4与ⅡA族元素性质相似
B、A113与卤素性质类似
C、A113在气态中与HI反应的方程式可表示为:A113+HI=HAl13I
D、A113超原子中A1原子间是通过离子键结合的
5、碘化砹(AtI)可发生下列反应,①2AtI+2Mg==MgI2+MgAt2
②AtI+2NH3(l)==NH4I+ AtNH2。对上述两个反应的有关说法正确的是
A、反应①MgAt2既是氧化产物,又是还原产物
B、这两个反应都是氧化还原反应
C、反应②中AtI既是氧化剂,又是还原剂
D、MgAt2的还原性弱于MgI2的还原性
4、据悉,奥运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生的化学方程式为: 5KClO3 + 6P== 3P2O5 + 5KCl ,则下列有关叙述错误的是
A、上述反应中氧化剂和还原剂的物质的量之比为5:6
B、产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾)
C、上述反应中消耗3molP时,转移电子的物质的量为15mol
D、因红磷和白磷互为同分异构体,所以上述火药中的红磷可以用白磷代替
3、关于某溶液所含离子检验的方法和结论正确的是
A、加入过量NaOH溶液,有白色沉淀生成,则原溶液一定有Mg2+
B、加入AgNO3溶液有白色沉淀生成,加稀盐酸沉淀不消失,则原溶液一定有Cl-
C、加入盐酸产生能使澄清石灰水变浑浊的气体,则原溶液中可能有
CO32-或SO32-
D、加入NaOH并加热,产生使湿润的蓝色石蕊试纸变红的气体,则原溶液是铵盐溶液
2、下列有关说法不符合事实的是
A、同温同压下,气体的体积取决于气体的物质的量的多少
B、元素的相对原子质量取决于该元素各核素的相对原子质量和在自然界中的原子百分比
C、氯化钠投入到酒精中将形成胶体
D、氧化剂的氧化性强弱取决于该氧化剂中某元素化合价的高低
1、2006年9月21日,美国亚特兰蒂斯号航天飞机在爱德华空军基地安全着落,航天飞机表层的防热瓦曾成为航天飞机能否安全着落的制约因素。防热瓦是以石墨材料为主要成分的非常疏松的泡沫陶瓷。下列有关说法合理的是
A、石墨成为该泡沫陶瓷主要成分的主要原因是石墨是原子晶体
B、石墨成为该泡沫陶瓷主要成分的主要原因是石墨熔点很高
C、石墨中碳碳键之间的夹角为109°28'
D、C60也可代替石墨用作航天飞机表层的防热瓦材料
29.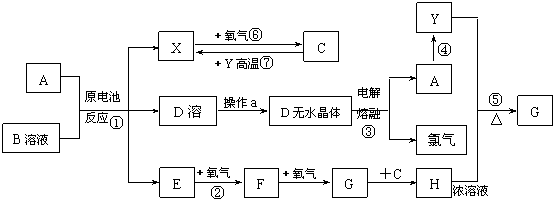 (10分)已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质)。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图:
(10分)已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质)。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图:
(注意:其中有些反应的条件及部分生成物被略去)
请填写下列空白:
(1)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为
(2)从D溶液制备D的无水晶体的“操作a”为 。
(3)反应②的化学方程式为 。
(4)反应⑤的化学方程式为 。
(5)原电池反应①中正极的电极反应式为 。
28.(Ⅰ)(8分)A为苯的二元取代物,只含有C、H、O三种元素,A的相对分子质量为150;A不能使FeCl3溶液显色,也不能发生消去反应,但可以被新制Cu(OH)2氧化为B;B能在浓硫酸存在和加热时发生分子内的酯化反应生成C,C分子中有一个含氧的六元环。
(1)符合条件的A的结构简式为_________________________。
(2)A与新制Cu(OH)2反应的化学方程式为:
_______________________________________________________________
(3)B中含有的官能团的名称为__________和___________,B生成C的化学方程式为:
______________________________________________________________
(Ⅱ).我国盛产山茶子精油,用其主要成分柠檬醛可以与丙酮反应制取假紫罗兰酮,进而合成具有工业价值的紫罗兰酮。
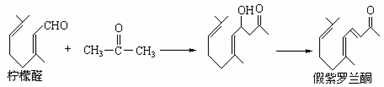 又知:R-X+H2O®R-OH+HX(“R-”为烃基)
下面是一种有机物A的合成路线,请回答有关问题:
又知:R-X+H2O®R-OH+HX(“R-”为烃基)
下面是一种有机物A的合成路线,请回答有关问题:
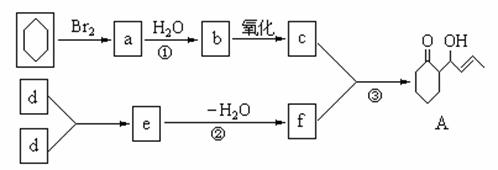
(1)写出c、d、f的结构简式:c d f
(2)指出反应类型:① ② ③
(3)下列关于有机物A化学性质正确的有( )
①在一定条件下1molA能与2molH2发生加成反应
②1molA与足量钠反应产生1mol H2
③1molA能与2molBr2发生加成反应
④1molA充分燃烧消耗12.5mol氧气
27.用化学方法测定微量碘化物时,须先利用“化学放大”反应将碘的量“放大”,然后再进行测定。下面是两次“化学放大”反应的实验步骤:
①向含微量I-并且呈中性或弱酸性溶液里加入溴水,将I-完全氧化成IO-3 ,煮沸去掉过量的Br2;
,煮沸去掉过量的Br2;
②向由①制得的水溶液中加入过量的酸性KI溶液,振荡使反应进行完全;
③在②得到的水溶液中加入足量的CCl4,振荡,把生成的I2从水溶液里全部转移到CCl4中,用分液漏斗分液去掉水层;
④将③得到的CCl4层加入肼(即联氨H2NNH2)的水溶液,振荡,使I2完全以I-形成从CCL4层进入水层,用分液斗分液去掉CCl4层;
⑤向由④制得的水溶液中加入过量的溴水,重复上述步骤①;
⑥向由⑤制得的水溶液中加入过量的酸性KI溶液,重复步骤②;
⑦向由⑥得到的水溶液加入足量的CCl4,重复步骤③;
⑧向由⑦得到的CCl4层加入肼的水溶液,重复步骤④。
经过以上过程得到的水溶液里含有通过反应而“放大”了的碘,请回答下列问题:
(1)完成并配平下列指定反应的离子方程式
①在水溶液里,I-被Br2氧化成IO3-的反应:
□I-+□Br2+□H2O=□IO3- + □H++□__
②在酸性溶液里,I-被IO3-反应生成I2的反应:
□IO3-+□I-+□__=□I2 + □H2O
(2)配平I2与肼反应的离子方程式,并表示出该反应的电子转移的方向和数目。
□I2+□H2NNH2=□H++ □I-+ □N2↑
 (3)将右图所示的分液漏斗中下层液体放出的操作步骤为:
(3)将右图所示的分液漏斗中下层液体放出的操作步骤为:
ⅰ. 。
ⅱ.旋开活塞,使下层液体流出到一个烧杯里,当下层液体全部流
出活塞的细孔时,迅速关闭活塞。
ⅲ. 。
ⅳ. 。
(4)若忽略过程中出现的损失,经过一次“化学放大”的溶液里,I-的
量是原溶液里I-的量的 倍。经过n次“化学放大”的溶液里I-
的量是原溶液里I-的量的 倍。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com