
题目列表(包括答案和解析)
16.(10分)(1)有常用玻璃仪器组成的下列六种实验装置(根据需要可在其中加入液体或固体)
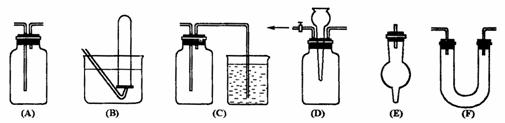
①能用做干燥二氧化硫气体的装置有 ;(填代号,下同)
②既能用于收集氯气又能用于收集一氧化氮气体的装置有 ;
③在氯气和铁反应实验中,能添加在制气和化合反应装置之间以除去氯气中氯化氢等杂质气体的装置有 ;
④在乙烯与溴水反应制二溴乙烷的实验中,能添加在制乙烯装置和加成反应装置之间,达到控制气流使其平衡目的的是 ;
⑤若用C装置做二氧化硫与烧杯中氢氧化钠溶液反应实验,则其中广口瓶的作用是 。
15. 500℃、20Mpa时,将H2和N2置于一容积为
500℃、20Mpa时,将H2和N2置于一容积为
2L的密闭容器中发生反应。反应过程中H2、N2
和NH3物质的量变化如图所示,下列说法正确
的是( BC )
A.反应开始到第一次平衡时,N2的平均反应速
率为0.005mol/(L·min)
B.从曲线变化可以看出,反应进行到10min至
20min钟时可能是使用了催化剂
C.从曲线变化可以看出,反应进行至25min钟时,
分离出0.1mol的氨气
D.在25min钟时平衡正向移动但达到新平衡后
NH3的体积分数比原平衡小
第Ⅱ卷 (非选择题共90分)
13.将等浓度的K2S溶液和NaHSO4溶液等体积混合,得到的溶液中离子浓度关系正确的是(CD)
A.c(K+)>c(Na+)> c(H+)>c(OH-)
B.c(Na+)+ c(K+)+ c(H+)= c(SO42-)+ c(HS-)+ c(OH-)+c(S2-)
C.c(SO42-)> c(HS-)> c(OH-)> c(H+)
D.c(K+)=c(S2-)+ c(H2S)+c(HS-)+c(SO42-)
14.铁粉和铜粉的均匀混合物,平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只有NO):
|
编号 |
① |
② |
③ |
④ |
|
稀硝酸体积/mL |
100 |
200 |
300 |
400 |
|
剩余金属/g |
18.0 |
9.6 |
0 |
0 |
|
NO体积/mL |
2240 |
4480 |
6720 |
V |
下列计算结果正确的是(BD)
A.①中溶解了5.6gFe B.硝酸的浓度为4mol/L
C.②中溶解了9.6gCu D.④中V=8960
12.化学中常用类比的方法可预测许多物质的性质。如根据H2+Cl2=2HCl推测:H2+Br2=2HBr。但类比是相对的,如根据2Na2O2+2CO2= Na2CO3+ O2, 类推2Na2O2+2SO2= Na2SO3+ O2是错误的,应该是Na2O2+SO2= Na2SO4。 下列各组类比中正确的是(C)
A.由NH4Cl NH3↑+HCl↑,推测:NH4I
NH3↑+HCl↑,推测:NH4I NH3↑+HI↑
NH3↑+HI↑
B.由CO2+Ca(ClO)2+H2O=CaCO3↓+2HClO,推测:2SO2+Ca(ClO)2+H2O=CaSO3↓+2HClO
C.由2CO2+Ca(ClO)2+2H2O=Ca(HCO3)2+2HClO,推测:CO2+NaClO+H2O=NaHCO3+HClO
D.由Na2SO3+2HCl=2NaCl+H2O+ SO2↑,推测:Na2SO3+2HNO3=2NaNO3+H2O+ SO2↑
11.将质量为w1g的钠、铝混合物投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V1 L。向溶液中逐滴加入浓度为a mol/L的HCl溶液,过程中有白色沉淀生成后又逐渐溶解,当沉淀恰好消失时所加HCl溶液体积为V2 L。将溶液蒸干灼烧得固体w2g。下列所列关系式中正确的是 (BC)
A.35.5a V2 =w2-w1 B.23n(Na)+27n(Al)=w1
C.n(Na)+3n(Al)=2V1/22.4 D.a V2 =V1/22.4
10.某一元弱酸HA的相对分子质量为M。在t℃时,将a gHA完全溶解于水,得VmL饱和溶液,测得该溶液的密度为ρg·cm-3,其中n(A-)为bmol。下列叙述,错误的是 ( C)
A.溶液中c(H+)
=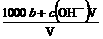 B.物质的量浓度c(HA) =
B.物质的量浓度c(HA) =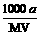 mol·L-1
mol·L-1
C.t℃时,HA的溶解度S=100a/ρV D.HA的质量分数w(HA) = a/ρV ╳ 100%
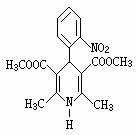
9.硝苯地平缓释片(Nifedipine Sustained Release Tablets)用于治疗各种类型的高血压及心绞痛,其结构式如右图所示:
下列关于硝苯地平缓释片的说法正确的是(C)
A.硝苯地平缓释片的分子式为C17H17N2O6
B.1mol硝苯地平缓释片在水溶液中最多能消耗4molNaOH
C.1mol硝苯地平缓释片在一定条件下能和5molH2发生加成反应
D.硝苯地平缓释片中N的化合价为-3
8.下列离子方程式书写正确的是( C)
A.碳酸氢钠溶液中加入少量的石灰水:HCO3-+Ca2++OH-=CaCO3↓+H2O
B.稀醋酸溶液中加入少量的铁粉:2H++Fe = Fe2++H2↑
C.将饱和FeCl3溶液滴入沸水中:Fe3++ 3H2O = Fe(OH)3(胶体) + 3H+
 D.氯化钙溶液中通入二氧化碳气体:Ca2++CO2+H2O=CaCO3↓+2H+
D.氯化钙溶液中通入二氧化碳气体:Ca2++CO2+H2O=CaCO3↓+2H+
7.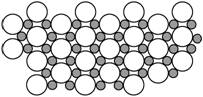 人们发现硼化镁在39 K时呈超导性,可能是人类对超导认识的新里程碑。在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼的相间排列,右图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。根据右图确定硼化镁的化学式为( B )
人们发现硼化镁在39 K时呈超导性,可能是人类对超导认识的新里程碑。在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼的相间排列,右图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。根据右图确定硼化镁的化学式为( B )
A.MgB B.MgB2 C.Mg2B D.MgB6
6.实验室保存下列试剂,其中保存方法和理由描述都正确的是 ( B )
|
编号 |
试 剂 |
保存方法 |
理 由 |
|
A |
固体氢氧化钠 |
存放在带橡皮塞的广口瓶中 |
防止空气接触被氧化,防止和水蒸气、二氧化碳接触而变质 |
|
B |
碳酸钠晶体 |
存放在干燥密封的广口瓶中 |
防止风化成粉末而变质 |
|
C |
液溴 |
存放在带橡皮塞的细口瓶中 |
防止挥发 |
|
D |
硝酸银溶液 |
存放在无色玻璃塞的试剂瓶 中,放在冷暗处 |
防止见光分解 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com